2026-03-24
对于罕见病领域,尤其是难治性癫痫的治疗,我们正迎来一个激动人心的时代。近日,来自得克萨斯大学西南医学中心的研究团队在知名医学期刊《The Journal of Clinical Investigation》(JCI)上发表了一项突破性的临床前研究:AAV-mediated gene therapy in a SLC13A5 citrate transporter disorder model rescues epileptic and metabolic phenotypes。该团队开发了一种腺相关病毒(AAV)介导的基因疗法,在SLC13A5柠檬酸转运蛋白缺陷模型小鼠中,成功挽救了严重的癫痫发作和代谢表型。
什么是SLC13A5柠檬酸转运蛋白障碍?
SLC13A5柠檬酸转运蛋白障碍是一种极其罕见的常染色体隐性遗传性癫痫性脑病。这种疾病非常残酷,患儿通常在出生后的第一天就会出现癫痫发作,并伴随终身的智力发育迟缓和运动障碍。
该疾病是由SLC13A5基因的功能丧失突变引起的。SLC13A5基因负责编码一种钠依赖性柠檬酸转运蛋白(NaCT),主要负责将细胞外的柠檬酸转运到神经元和星形胶质细胞内部,参与细胞能量代谢和神经递质的合成。当NaCT失去转运功能时,会导致患者血液和脑脊液中的柠檬酸水平异常升高,引发频繁的癫痫发作。目前临床上只有缓解症状的手段,急需一种能从根源上解决蛋白功能缺失的治愈性疗法。
打造基因“运钞车”:优化的AAV载体元件设计
在基因治疗中,载体调控元件的筛选与优化往往决定了药物在临床转化中的表达活性。为了实现高效的基因替代,研究团队精心设计了名为AAV/UsP-SLC13A5的表达载体。
表达元件的优化:该载体采用了一个泛表达的微型合成JeT加内含子启动子(UsP),用于驱动经过密码子优化的、带有合成polyA尾(SpA)的人类SLC13A5 cDNA表达 。这种设计旨在确保靶向组织中实现高效的转录与翻译。
自身互补(scAAV)的构建:受限于AAV的包装容量,短小精悍的UsP启动子使得全长1.7kb的SLC13A5编码序列得以被包装成自身互补AAV(scAAV)结构。通过突变一侧的反向末端重复序列(ITR),该设计引导了DNA序列的优先复制和包装。相比传统的单链AAV,scAAV能够实现更快、更稳定的转基因表达。
体外功能验证:该载体被包装在具有广泛中枢神经系统趋向性的AAV9衣壳中。在体外人类细胞测试中,该载体成功使NaCT定位于细胞膜(图1B-D),并在2小时内将培养基中的细胞外柠檬酸丰度降低了约70%(图1E),证实了转运功能的成功恢复。
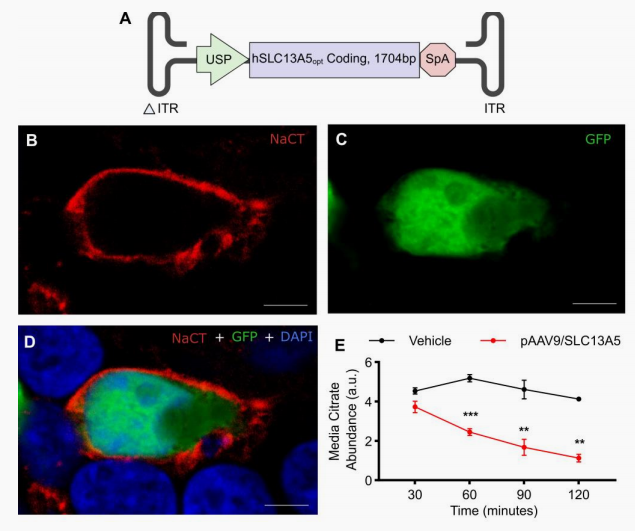
图1 AAV/SLC13A5载体设计、细胞表达及功能研究(图片来源:Bailey LE et al, J Clin Invest., 2026)
早期干预(P10):代谢表型与神经电生理的双重逆转
研究团队使用敲除Slc13a5基因的小鼠(KO小鼠)进行了体内药效学评价。在小鼠出生后第10天(P10),研究人员通过鞘内注射(IT)递送了低剂量(2×1010vg)或高剂量(8×1011vg)的AAV9/SLC13A5。
代谢拯救:治疗2个月后,KO小鼠异常升高的血浆柠檬酸水平呈剂量依赖性下降,低剂量组降至野生型(WT)的87%,高剂量组大幅降至65%(图2C)。脑脊液中的柠檬酸水平也显著回落至WT的81%。
癫痫遏制:基因治疗显著减少了小鼠大脑中的异常癫痫样放电棘波序列(图3B)。在戊四唑(PTZ)诱发测试中,治疗组小鼠的癫痫发作严重程度显著降低,发作潜伏期大幅延长。在8次PTZ诱导后,未治疗的KO小鼠死亡率达29%,而基因治疗有效保护了小鼠,极大降低了致死率(图3H)。
睡眠改善:治疗成功使小鼠在光照周期(睡眠期)的异常过度活动正常化,并剂量依赖性地增加了快速眼动睡眠(矛盾睡眠)的时间(图4F)。
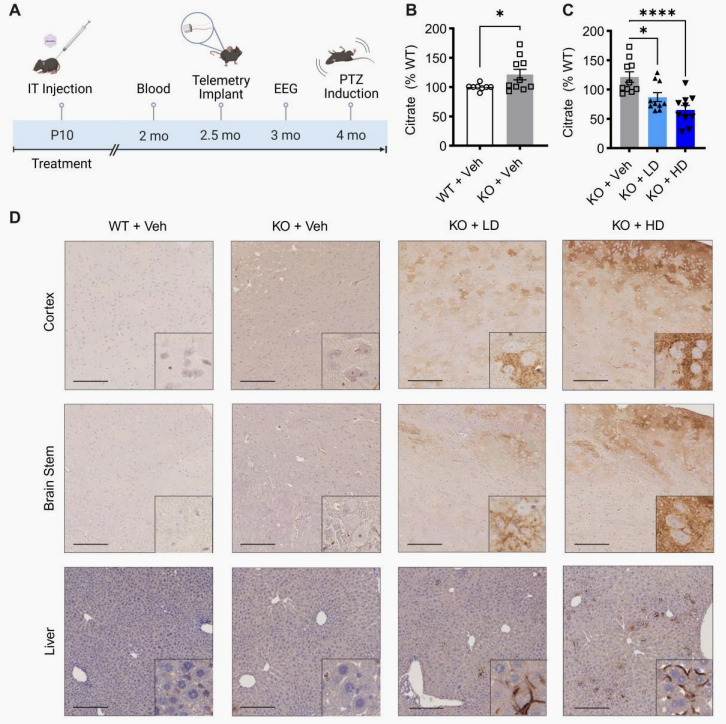
图2 在Slc13a5 KO小鼠出生后第10天(P10)进行脑室内(IT)注射AAV9/SLC13A5后,小鼠大脑中钠-柠檬酸共转运体(NaCT)表达显著增强,且血柠檬酸水平下降。(图片来源:Bailey LE et al, J Clin Invest., 2026)
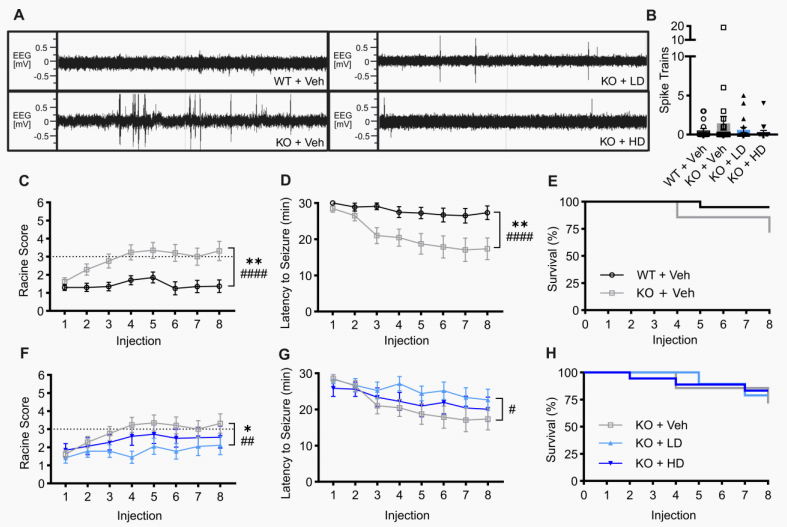
图3 AAV9/SLC13A5基因疗法在P10时对Slc13a5 KO小鼠进行治疗,成功缓解了其癫痫症状。(图片来源:Bailey LE et al, J Clin Invest., 2026)
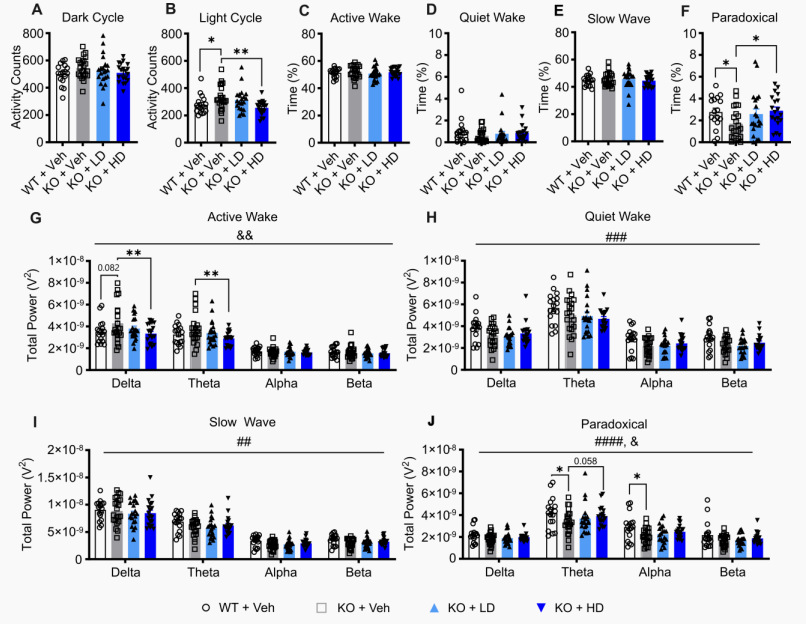
图4 P10时对Slc13a5 KO小鼠进行脑室内注射AAV9/SLC13A5,可纠正其异常的脑电图(EEG)睡眠特征。(图片来源:Bailey LE et al, J Clin Invest., 2026)
突破年龄限制:成年期干预的给药途径对比
很多神经发育疾病一旦错过早期窗口期便难以治疗。然而,当研究人员在3个月大的成年KO小鼠中进行实验时,依然观察到了惊艳的疗效。研究直接对比了两种给药途径:小脑延髓池注射(ICM)与腰椎鞘内注射(IT)。
靶向效率:ICM途径在成年小鼠大脑皮层、脑干和小脑中实现了比IT途径更广泛的NaCT蛋白表达(图5D)。ICM组将血浆柠檬酸水平降至WT的93.3%,IT组降至73.7%。
癫痫逆转:ICM途径递送的基因疗法完美地将成年KO小鼠异常的脑电活动恢复到了野生型正常水平(图6A)。成年期干预显著降低了PTZ诱发的癫痫严重程度,ICM和IT两种途径均将癫痫相关死亡率大幅控制在了17%(图6H)。
睡眠生理改善:8个月大的老年KO小鼠表现出清醒时间过少、慢波睡眠过多的异常 。基因治疗呈现出增加主动清醒时间的趋势,其中脑部转导率更高的ICM途径极为有效地降低了清醒期的异常慢波(Delta波)活动(图7E)。
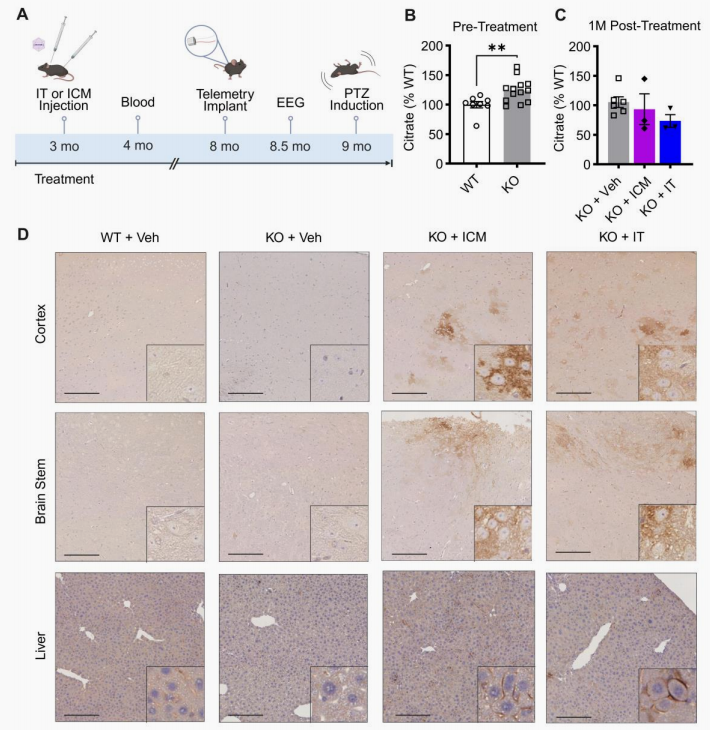
图5 与脑室内注射相比,在成年Slc13a5 KO小鼠中采用脑室内髓腔(ICM)注射AAV9/SLC13A5,可诱导大脑产生更高水平的NaCT。(图片来源:Bailey LE et al, J Clin Invest., 2026)
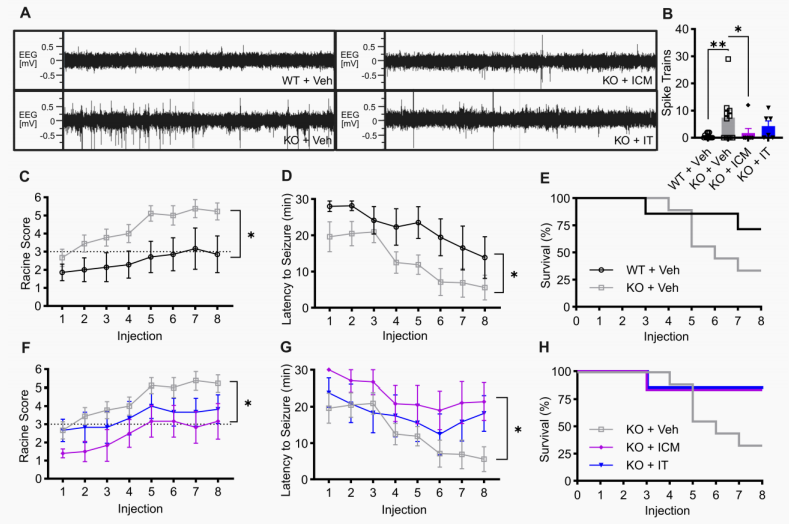
图6 与脑室内注射相比,在成年Slc13a5 KO小鼠中采用脑室内髓腔注射AAV9/SLC13A5,对癫痫表型的缓解效果更显著。(图片来源:Bailey LE et al, J Clin Invest., 2026)
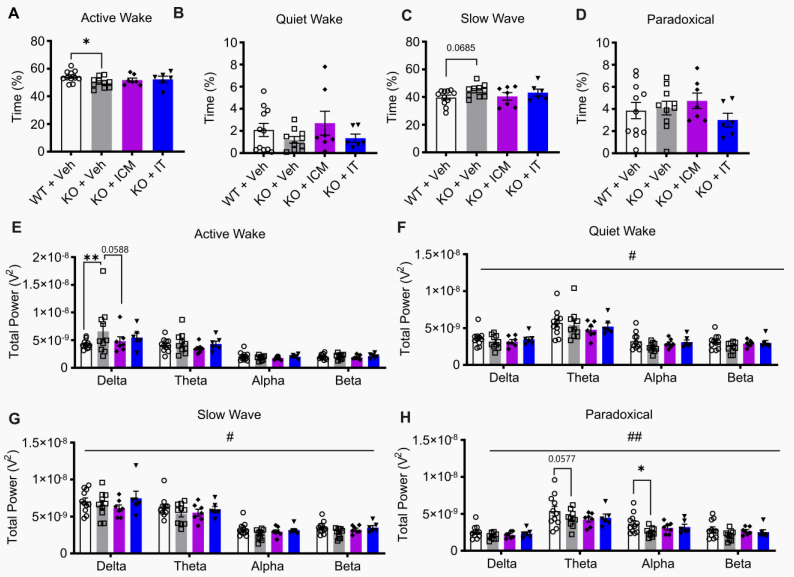
图7 AAV9/SLC13A5治疗可改善成年Slc13a5 KO小鼠的睡眠异常。
(图片来源:Bailey LE et al, J Clin Invest., 2026)
总结与临床转化前景
在安全性方面,无论是新生期还是成年期干预,AAV9/SLC13A5均表现出极好的耐受性。小鼠体重维持正常,且未引起任何肝肾功能损害,常规血液生化指标均在正常范围内。
这项研究强有力地证明:通过优化的调控元件设计,单次脑脊液注射AAV9基因疗法能够安全、持久地逆转SLC13A5缺陷小鼠的癫痫及代谢异常。更为振奋的是,其治疗时间窗甚至可以宽泛地延伸至成年期。这为该疗法迈向人类临床试验提供了坚实的科学基础。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。