2026-05-06
在基因治疗领域,重组腺相关病毒(rAAV)已成为递送DNA载荷的核心工具。然而,行业对AAV基础生物学认知的局限性,仍在制约相关疗法的开发速度。在rAAV的常规生产制造过程中,产生空壳或部分装载的衣壳是自然生命周期的一部分。这导致产品中经常混入无意中被封装的截短AAV基因组或DNA杂质。这些无治疗作用的截短基因组直接导致了产品的异质性,并会显著降低功能性载体的比例和最终的治疗效力。
关于导致这些异质性产物的底层因素,《Molecular Therapy: Nucleic Acids》上的一项研究提供了详实的分析。来自西班牙CIMA和美国UMass Chan医学院的科研团队,发表了题为《Orthogonal characterization of rAAV reveals vector attributes that drive ITR repair, self-complementary genome formation, and transgene expression》的研究论文。该团队通过多维度表征手段,系统评估了ITR设计、启动子序列以及AAV衣壳血清型对载体基因组异质性和转导效力的影响。
一、启动子序列特性:二级结构增加基因组截短风险
在表达载体的设计中,研究人员对比了两种常见的启动子组合:
AAT启动子:这是一种组织特异性启动子,构建的载体基因组大小约为2kb(图1A)。
CBA启动子:这是一种含有嵌合内含子的广泛表达型启动子,构建的载体基因组大小约为3kb(图1A)。
研究结果显示,无论是在AAV5、AAV8还是AAVLK03血清型中,携带CBA启动子的载体均表现出了更加显著的条带异质性和截短现象(图1C, 1D)。通过长读长单分子实时(SMRT)测序分析,研究确认CBA启动子和嵌合内含子区域以及HGH polyA区域存在大量的截短“热点”(图2B, 2D) 。特别是在装载临床相关基因SMN1时,含有CBA启动子的产品中,有57%的包装基因组发生了截短(补充图S2)。
导致这种大规模截短的核心诱因在于序列本身的物理特性,而非其广谱表达的生物学功能。研究明确指出,CBA启动子以及CMV增强子序列中富含复杂的二级结构(如发卡样结构)。在AAV基因组的复制或包装过程中,这些复杂的物理结构会引发强烈的空间阻碍,直接触发并导致载体基因组的分子截短。相比之下,AAT启动子序列并未引发此类大规模截短事件,其截短事件被大幅减少。这提醒研发人员,在载体序列设计时,必须高度警惕DNA序列空间二级结构对基因组完整性造成的负面物理影响。
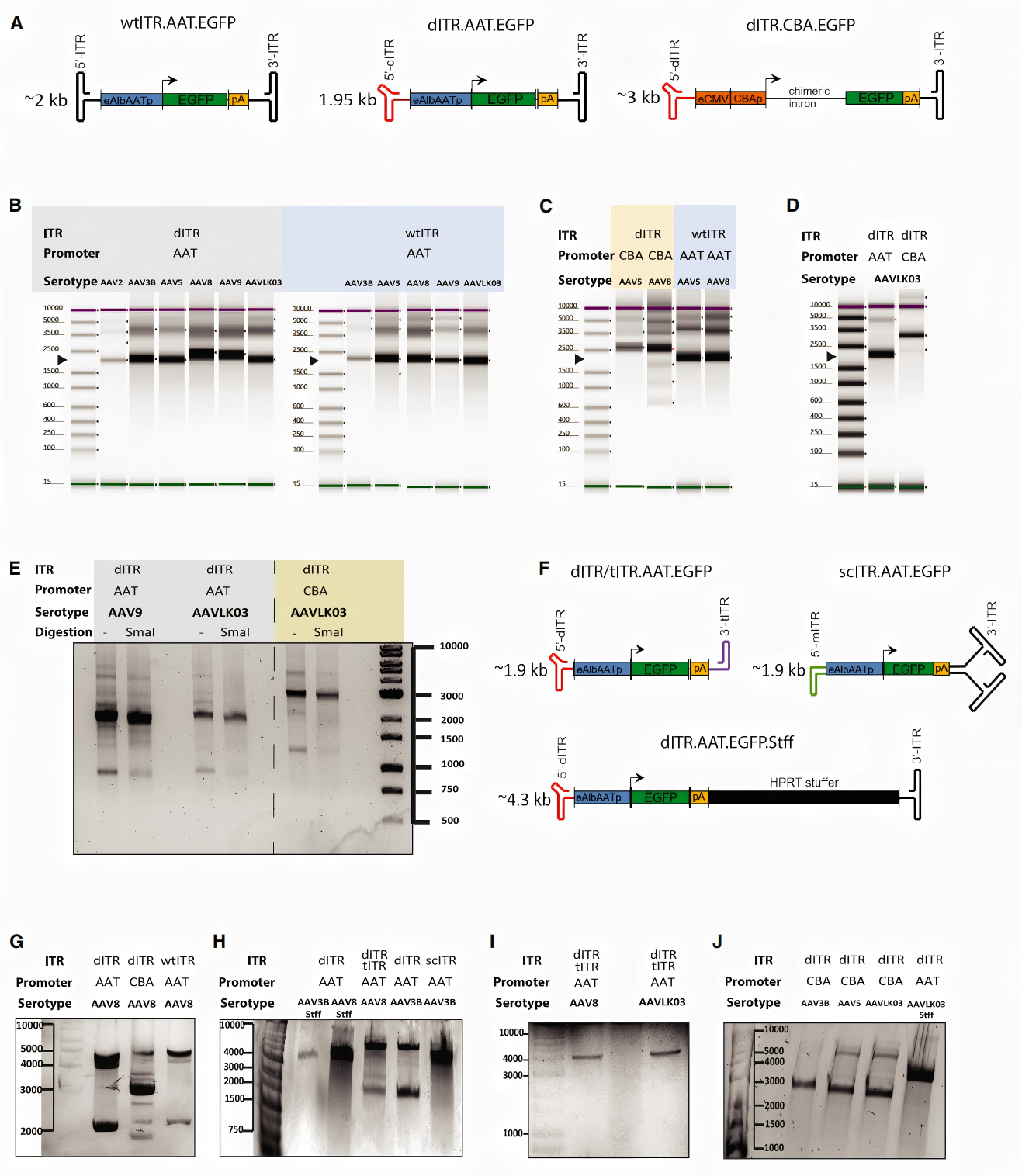
图1 天然电泳与碱性电泳解析重组AAV基因组元件及异质性特征
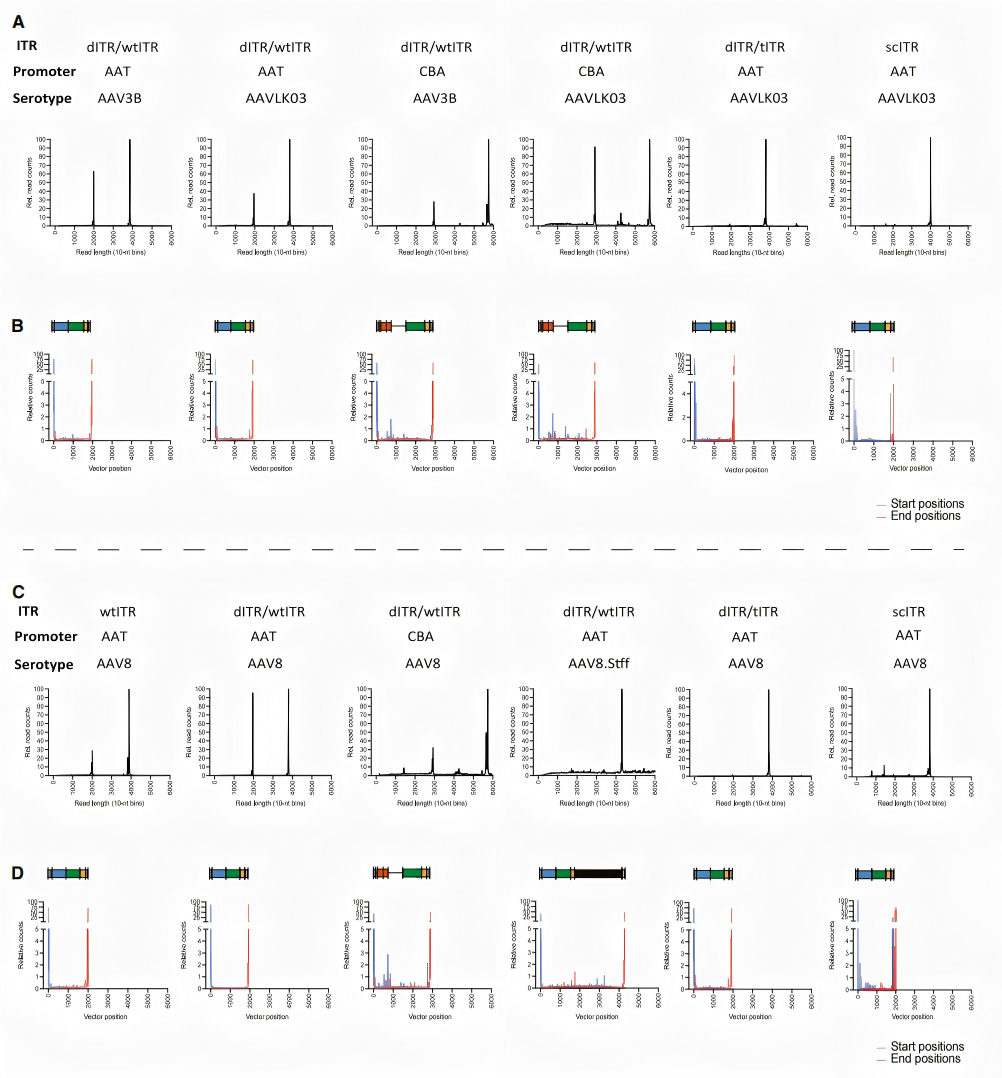
图2 基于长读长单分子实时(SMRT)测序的重组AAV基因组元件功能及异质性分析
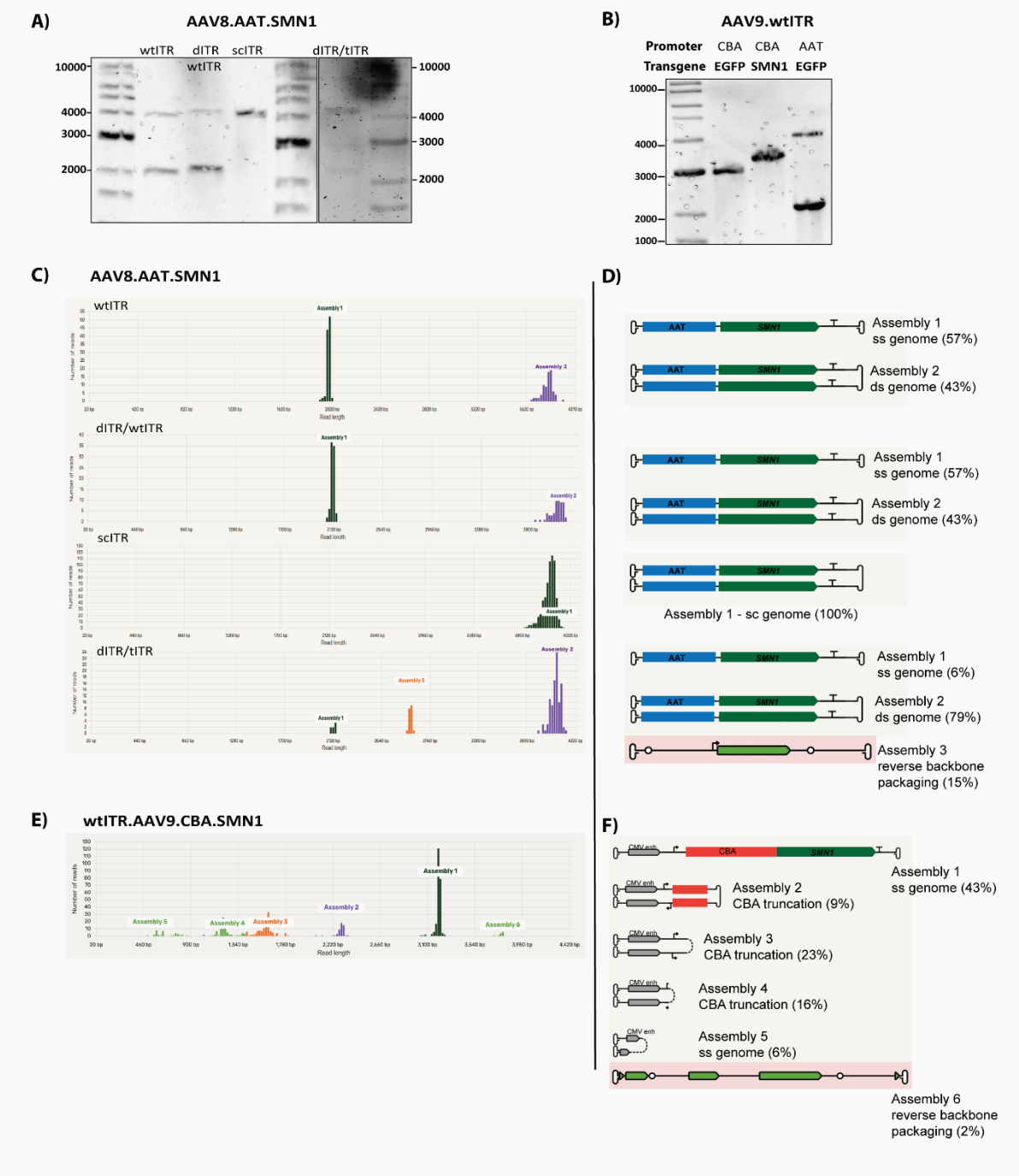
图S2 基于碱性电泳与长读长单分子测序的重组AAV.SMN1基因组异质性分析
二、ITR的修复机制与非典型大尺寸双链基因组的发现
ITR(反向末端重复序列)是对rAAV基因组正确包装必不可少的病毒原生序列。研究团队测试了多种ITR突变组合,包括:野生型(wtITR)、删除了11个核苷酸的dITR、删除了22个核苷酸的tITR,以及缺乏末端解析位点(trs)的自我互补scITR(图1F)。
实验观察到,在AAV复制过程中,ITR的微小截短缺陷会发生修复。例如,在dITR/tITR设计中,3'端的tITR有70%被转换成了5'端dITR的形态,同时还生成了少量的全新wtITR形式(图4B-4D)。这种修复效率深刻地受到载体基因组长度的影响:对于较短的紧凑型AAT启动子基因组,向wtITR的修复率超过70%;而对于包含CBA启动子或填充序列的较长基因组,修复率几乎接近100%(图4B)。唯一的例外是scITR设计,尽管存在3'端的wtITR作为模板,scITR也完全未发生任何形式的修复(图4B)。研究推测这是由于其能够生成高度稳定且更具效力的自我互补(sc)功能性基因组,从而在复制中占据了选择性优势。
在自我互补(sc)基因组的尺寸限制方面,传统观点认为其受限于AAV的包装容量(通常小于3.3kb)。但在该研究中,通过碱性凝胶和长读长测序,在特定的衣壳和ITR组合下发现了大于5kb甚至超过6kb的未解析基因组二聚体(图1J, 图2A-2C)。DNase和Benzonase酶切实验证实,这些大尺寸基因组具有酶抗性,在经过标准消化程序后依然存在,这表明它们至少有一部分是受到了AAV衣壳的物理保护,并被包装入内(表1, 表2, 补充图S3)。
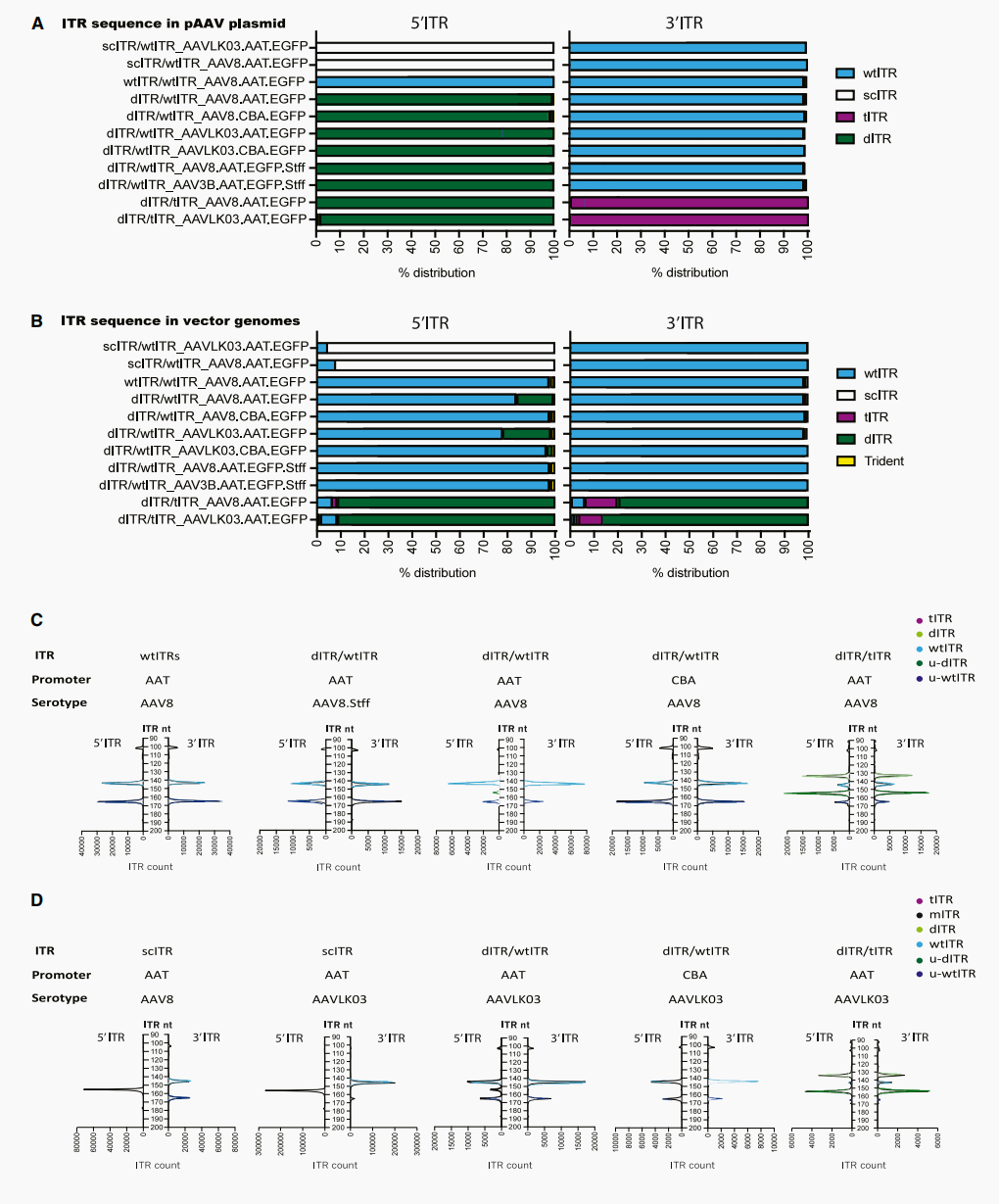
图4 代表性重组AAV载体的ITR序列修复机制分析
表1 DNase I酶处理前,AAV8与AAVLK03载体制备产物的DNA浓度检测
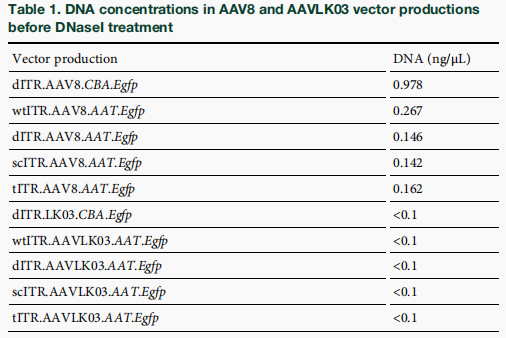
表2 DNase I与苯宗核酸酶(Benzonase)处理前后,添加外源DNA的AAV8与AAVLK03载体制备产物中的DNA浓度
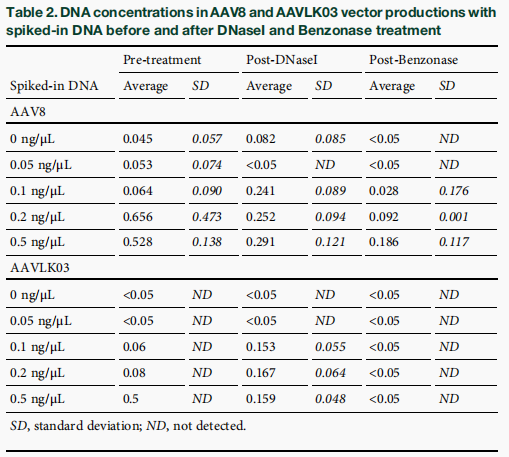
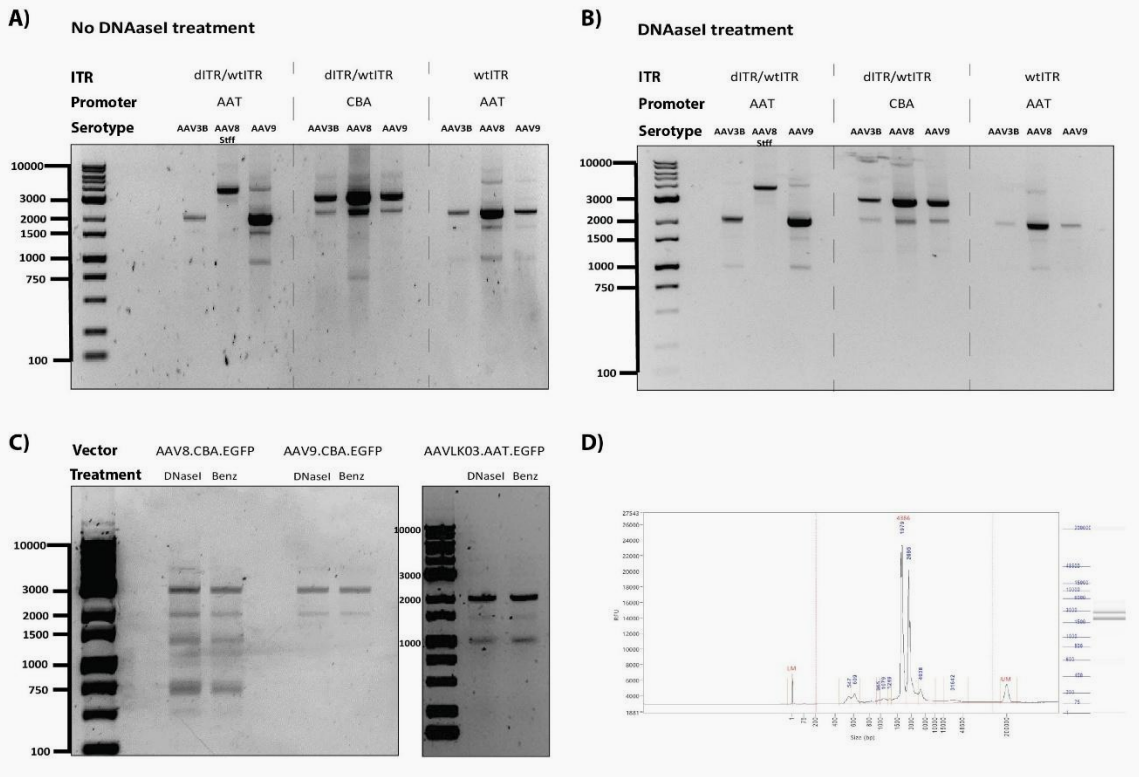
图S3 A)DNase I酶切前,提取AAV3B、AAV8、AAV9血清型重组AAV基因组,通过天然琼脂糖凝胶电泳,对比AAT启动子与CBA启动子、缺陷型ITR与野生型ITR的差异;B)DNase I酶切后,对AAV3B、AAV8、AAV9血清型rAAV基因组进行天然琼脂糖电泳,对比不同启动子(AAT/CBA)与不同ITR(dITR/wtITR)的表达差异;C)经DNase I或苯宗核酸酶(Benzonase)消化处理后,AAV8、AAV9、AAVLK03血清型rAAV基因组的天然琼脂糖电泳检测;分子量标准:FastGene 1-kb DNA标志物(分子量区间:100-10000bp);D)AAVLK03载体基因组经提取后,于单分子实时(SMRT)测序前,完成2kb与3kb混合片段的片段化分析。
三、衣壳血清型差异:AAV8与AAVLK03对基因组完整性的不同影响
AAV衣壳在ITR修复和基因组包装中发挥着至关重要的相互作用。研究对比了AAV8和高嗜肝性突变体AAVLK03两种血清型的表现:
AAV8的特征:AAV8生产的载体产量虽然较高,但在其提取的基因组中,存在高比例的“未解析野生型ITR(u-wtITR)”(图4C)。这意味着依赖Rep蛋白的末端解析过程失败或不完全,导致包装了大量复制中间体,这一现象在携带CBA启动子时尤为丰富,加剧了异质性。在DNase处理前,AAV8制剂中即可检测到0.14至0.9ng/μL的DNA(表1)。
AAVLK03的特征:无论搭配哪种基因组特征,AAVLK03包装出的未解析ITR比例始终显著偏低(图4D)。DNase处理前后的定量数据显示,AAVLK03制剂中的游离DNA水平始终低于检测限(表1, 表2)。数据提示,AAVLK03在包装和解包解析后的功能性双链载体方面可能具备极高的效率,这需要依赖入胞后的衣壳-ITR相互作用。
四、体内外表达差异:ITR与衣壳组合决定最终治疗效力
基因组的形态与完整性最终必须落脚到治疗效力上。研究评估了不同设计组合在体内外模型的转导表现:
小鼠体内实验(AAV8-SMN1):在静脉注射载体14天后,scITR构建体在小鼠肝脏中的SMN1 mRNA表达量最高,其次是dITR/tITR组合(图6A)。常规的wtITR和dITR/wtITR表达量最低,两者之间没有显著差异(图6A)。这在体内层面证实了具有双链sc基因组的设计拥有压倒性的效力优势。
体外细胞实验:在人类肝癌细胞系(Huh7)中,AAVLK03搭配dITR/tITR设计的表现展现了截然不同的动态(图5E-5G)。在最低剂量下,该组合的效力最强,超过了scITR;在达到转导平台期的高剂量下,其阳性细胞的荧光强度是其他设计的至少两倍以上(图5G)。这表明,功能性ITR修复与最终效力的提升不仅相关,而且高度依赖于特定的AAV血清型。
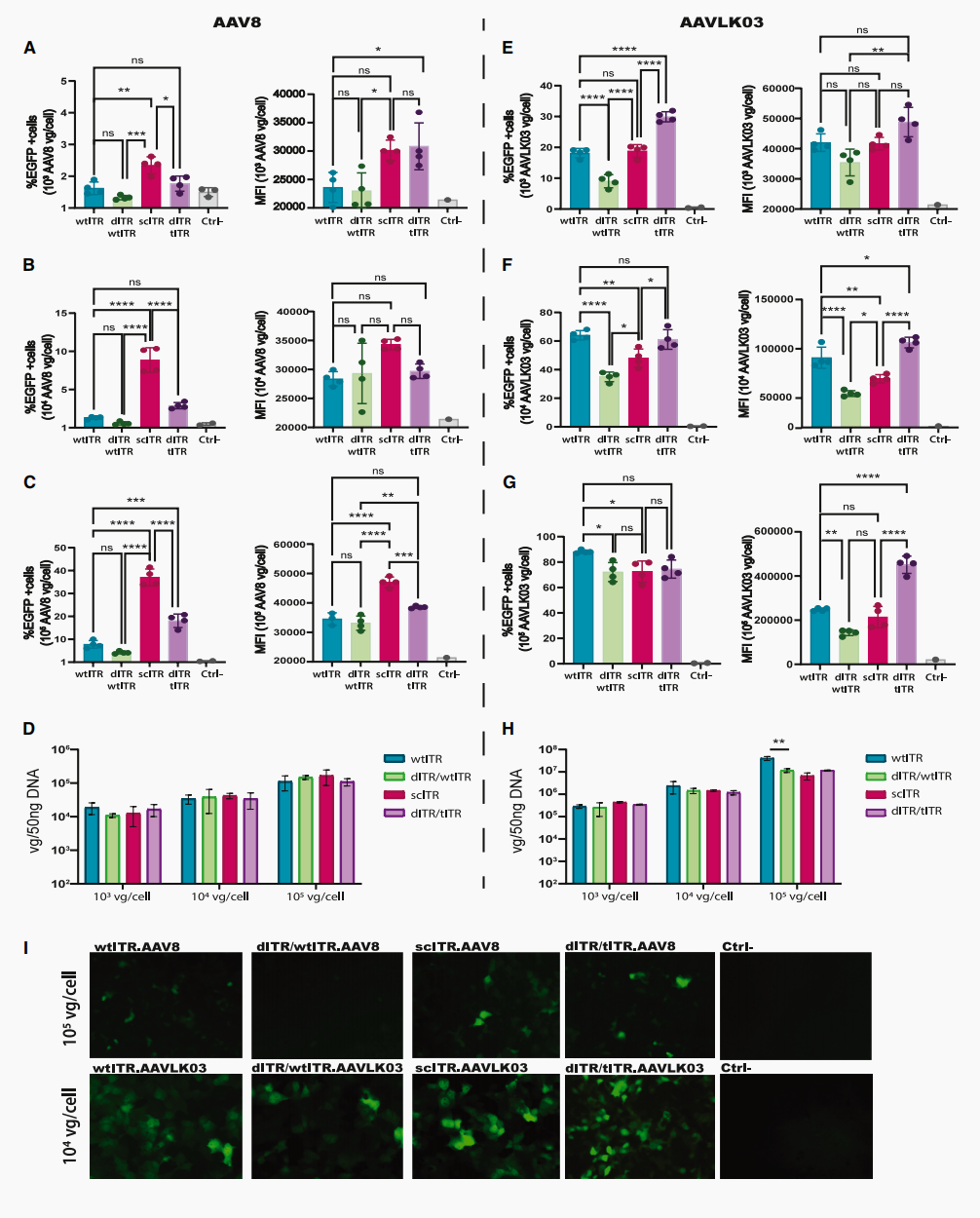
图5 不同ITR结构构型的重组AAV体外转导效率研究
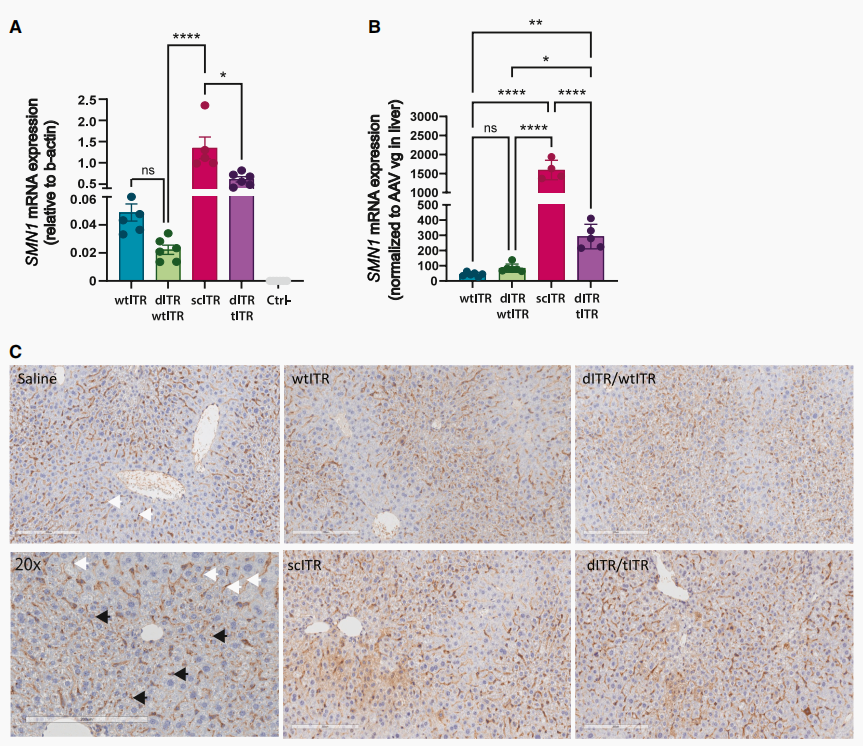
图6 携带不同ITR构型的rAAV8-SMN1载体体内功能表征
五、核心研究结论与研发建议
1.载体序列中的复杂二级结构(如CBA启动子区域的发卡样序列)是引发基因组大规模分子截短的物理根源。通过序列优化削弱或消除此类二级结构,是提升载体完整性的关键步骤。
2.缺陷型的ITR序列在AAV复制过程中会发生基于功能序列模板的自我修复。这种修复的效率及最终的ITR配置,受到基因组长度与特定衣壳血清型的双重且深刻的调控。
3.特定衣壳(如AAVLK03和AAV5)具备将超过传统尺寸限制(>5kb)的双链基因组二聚体进行物理包装和保护的能力。这些非典型大尺寸双链产物在工艺开发和质量评估中的潜在功能值得进一步关注。
4.长读长测序技术(如SMRT和Oxford Nanopore)能够以极高的灵敏度捕捉导致异质性的截短片段、反向包装以及各类杂质基因组。将该类技术纳入rAAV生产质控的常态化流程中不可或缺。
5.ITR的结构设计必须与具体的AAV血清型进行联合考量与匹配。正如dITR/tITR在AAVLK03中展现出了超越传统scITR设计的转导潜能,寻找特定衣壳的专属ITR组合是激发最大转导效力的核心策略。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。