2026-05-11
导读
法布雷病(Fabry disease)作为一种罕见的X连锁溶酶体贮积症,其常规的酶替代疗法(ERT)虽然能缓解部分系统性症状,但频繁的静脉输注、极短的药物半衰期以及高昂的成本,始终是临床应用中难以跨越的瓶颈。近日,国际遗传工程和生物技术中心(ICGEB)Andrés F. Muro课题组在遗传代谢病权威期刊《Journal of Inherited Metabolic Disease》发表重磅研究“Liver Gene Therapy in Fabry Disease Mice With Low Doses of rAAV2/8 Expressing a Codon-Optimized hGLA cDNA Results in Long-Term Disease Correction”,证实深度优化人源GLA基因序列后,仅需单次极低剂量(3.0×1011vg/kg)rAAV2/8载体递送,即可在模型小鼠中实现长期的生化底物清除与神经痛觉纠正,提供了极具吸引力的“低剂量、高效能”治疗方案。
1.突破传统ERT半衰期局限:AAV靶向肝脏递送展现长效替代潜力
法布雷病的核心病理在于GLA基因突变导致α-半乳糖苷酶A(α-Gal A)活性缺乏。酶活性的丧失会引发红细胞糖苷脂(Gb3)及其脱酰基形式(lyso-Gb3)在靶器官内进行性蓄积,导致广泛的多器官损害。
目前临床标准干预是定期静脉输注重组酶(ERT)。然而,该疗法重组酶半衰期极短,血药浓度剧烈波动,且患者极易产生抗药抗体严重削弱长期疗效。相比之下,利用AAV载体靶向肝脏的基因疗法展现出巨大优势。肝脏转导后能作为内源性“生物工厂”,全天候不间断合成并分泌功能正常的α-Gal A酶,随后被全身受累组织大量摄取,实现长效稳定的跨细胞病理纠正。
2.序列深度优化:筛选出兼具高表达与高分泌特性的GLA-CO2变体
为突破AAV包装限制并最大化蛋白表达效能,研究团队对人源野生型GLA mRNA序列进行了深度的综合密码子优化。通过精细调整靶标GC含量、消除潜在CpG岛与隐蔽剪接位点,成功构建出四个优化变体(hGLA_CO1-CO4),并克隆至携带肝脏特异性启动子(hAAT)的pSMD2载体中。
在Huh-7肝癌细胞系的体外测试中,优化后的CO1、CO2和CO3变体展现出远超野生型(WT)的性能:细胞上清液中的酶活性和靶蛋白丰度分别达到了WT序列的4倍和6倍,证实优化极大改善了靶蛋白的分泌效率。
随后在野生型小鼠体内评估确认:GLA-CO2变体在肝脏组织与血浆中诱导出的α-Gal A酶活性及蛋白表达量综合表现最为优异,被锁定为核心评估序列。
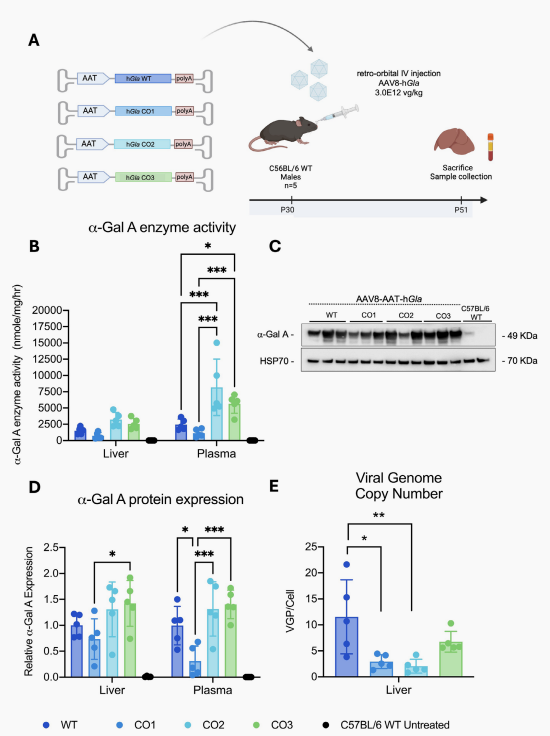
图1 野生型小鼠体内密码子优化序列的效果评估
3.活体药效验证:极低剂量单次给药的底物清除率远超高剂量ERT
在Gla基因敲除小鼠模型中,研究执行了活体剂量递增实验,设置了涵盖3.0×1011到3.0×1013vg/kg的四个给药梯度。平行对照组接受了达到人类常规临床剂量5倍的超高剂量ERT。
在实验终点(P150天),即使是3.0×1011vg/kg极低剂量GLA-CO2组,其血浆内α-Gal A酶活性也达未治疗健康小鼠的57倍,lyso-Gb3大幅下降89.5%。当剂量提升至3.0×1012vg/kg时,底物清除率高达98.1%。
在受累组织微环境层面,3.0×1011vg/kg剂量的GLA-CO2成功清除了肝脏、肾脏和心脏中分别95%、87%和84%的lyso-Gb3病理蓄积。反观5倍超高剂量高频注射的ERT治疗组,在这三个器官中的清除率分别仅有76%、67%和56%。这雄辩证明,单次低剂量AAV干预在逆转脏器底层代谢紊乱方面具备压倒性优势。
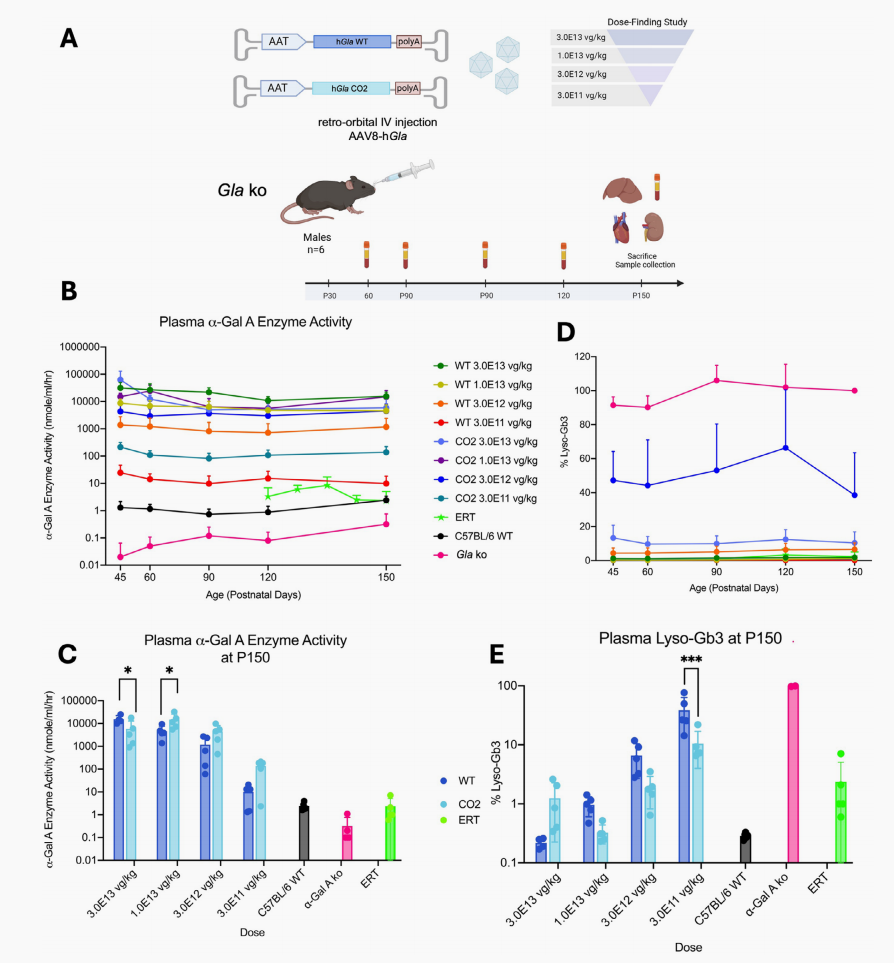
图2 经AAV基因治疗的法布雷病模型小鼠体内评价不同密码子优化cDNA变体的表现
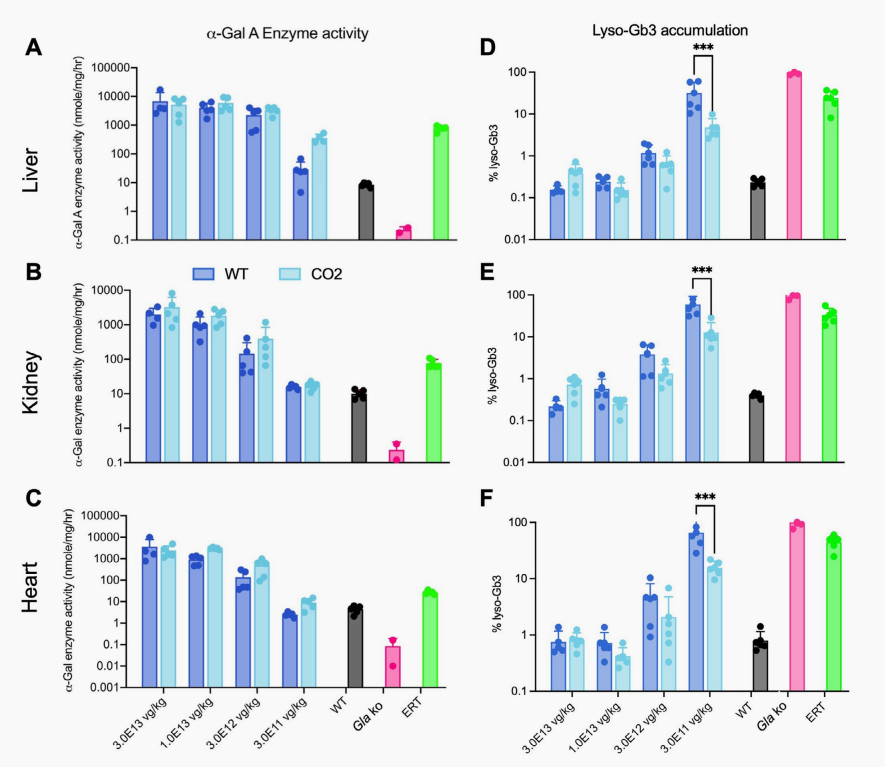
图3 经AAV基因治疗的法布雷病敲除小鼠各组织中目的酶活性和致病脂质lyso-Gb3沉积量
4.11个月长效追踪:生化指标持续平稳并全面逆转神经痛觉异常
为验证干预疗效的长期稳定性,研究设立观测队列,对接受3.0×1012vg/kg剂量GLA-CO2治疗的小鼠进行了长达11个月的监测。
在近一年的跨度内,受试小鼠血浆及核心脏器内的酶活性和lyso-Gb3降幅维持极其平稳,未见任何药效衰减。组织病理学切片直观证实,未治疗模型小鼠肝肾内大量深染的致病性Gb3沉积团块已被彻底清除,形态基本恢复健康状态。
针对法布雷病易伴发的周围神经病变,热板实验展示,未干预模型小鼠痛觉潜伏期达到健康小鼠的2至3倍,感觉迟钝。接受AAV-GLA干预的小鼠,痛觉潜伏期完全缩短并百分百恢复至正常基线水平,这确认底层代谢改善成功转化为神经系统缺陷的实质性逆转。
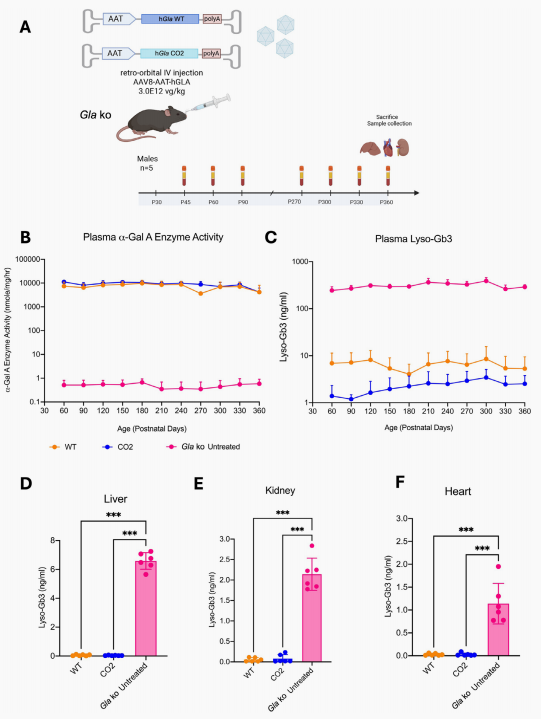
图4 长期随访经AAV基因治疗的法布雷病敲除小鼠疾病表型改善情况
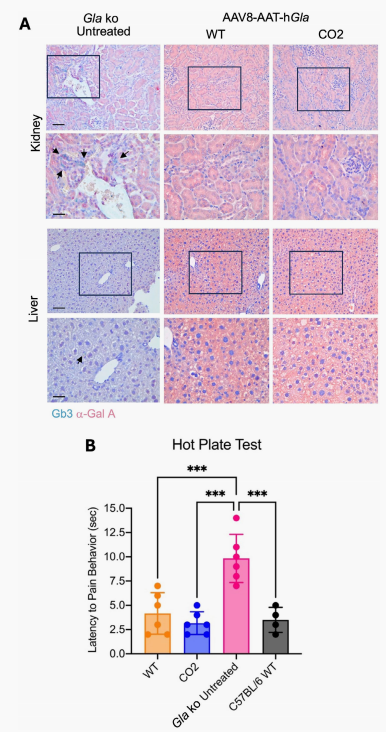
图5 长期随访经AAV基因治疗的法布雷病敲除小鼠的组织学与功能学评价
临床转化前景:降低有效给药滴度以规避高剂量AAV毒性风险
着眼于临床转化,本研究底层优化方案展现出了极高的“量效比”核心竞争力。当前处于开发阶段的多项同类法布雷病AAV基因疗法,普遍需要输入1.0×1013甚至1.0×1014vg/kg的高暴露剂量方能实现病理纠正。而本研究证明,通过密码子优化,在低至3.0×1011vg/kg的病毒滴度下即可强效清除84%至95%的有害代谢底物。
系统性输入高负荷AAV会呈指数级增加急性肝损伤、系统性免疫排斥及整合基因毒性风险。本研究所验证的极低剂量方案从源头上大幅减轻了病毒衣壳负荷,为长期忍受频发ERT输液折磨的患者群体,构筑了一条具备高度安全冗余的长效治愈转化路径。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。