2026-01-19
腺相关病毒(AAV)载体因其毒性极低且能够递送治疗基因,被广泛用于基因治疗。然而,相当一部分人体内已预先存在AAV中和抗体(NAb);这些抗体诱发的免疫反应不仅会影响AAV基因疗法的治疗效果,而且会给患者带来潜在的安全风险。因此,大多数基于AAV的基因治疗临床试验都会排除预先存在抗AAV NAbs的患者,抗AAV Nabs的存在也成为了限制基因治疗惠及患者的最大实际障碍之一。虽然这种排除对于静脉注射(i.v.)的AAV基因疗法而言完全合理,但AAV基因疗法还有许多其他给药途径,例如直接脑实质内注射、视网膜下注射或鞘内(IT)注射等。这些给药途径是否也应采取相同排除措施,一直是一个悬而未决的问题。
针对这一问题,Vono等人就非人灵长类动物(NHP)的AAV9鞘内给药进行了深入探讨,并发表在《分子治疗方法与临床开发(Molecular Therapy Methods & Clinical Development)》杂志上。该研究证实了以往研究已表明的结论:当AAV9经鞘内注射给药时,预先存在的抗AAV抗体不会抑制中枢神经系统(CNS)的生物分布,也不会造成任何重大的安全隐患。Steven J. Gray近期在同一期刊上发表的短评为我们介绍并分析了该项研究的成果。
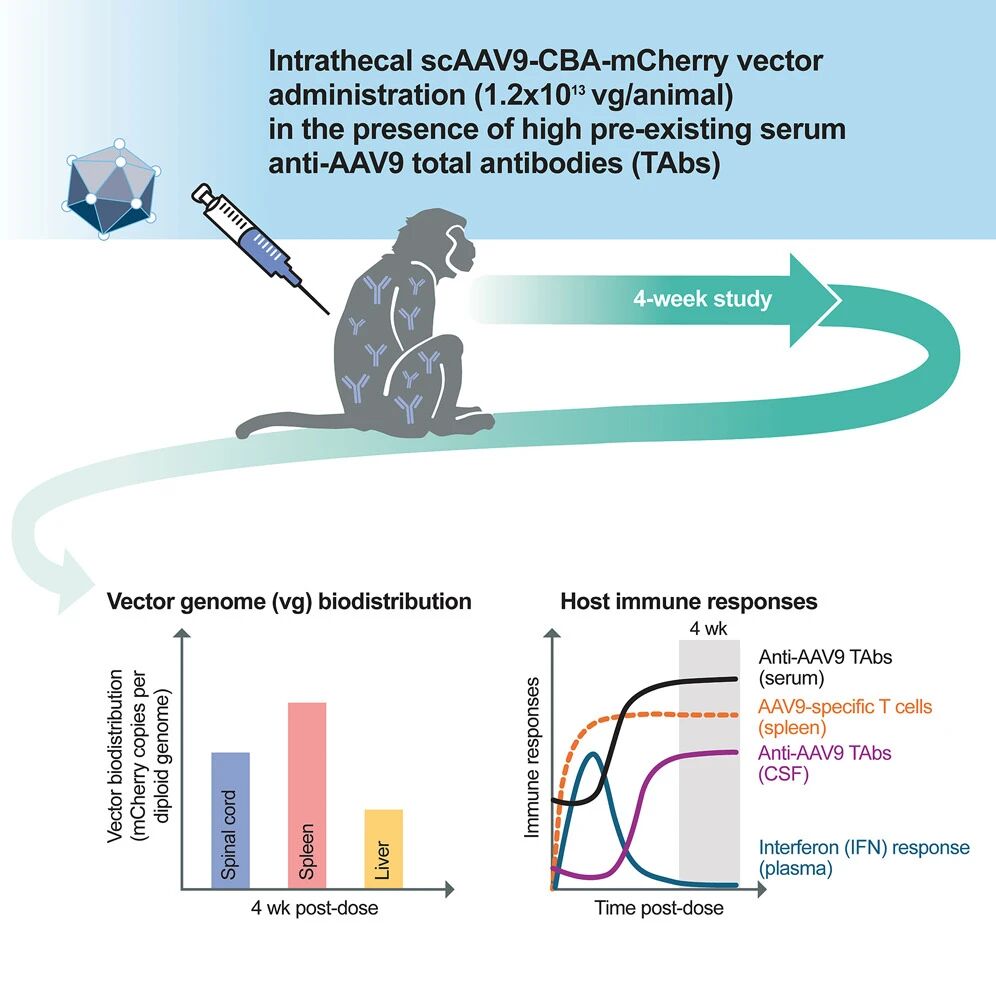
(图片来源:Maria Vono et al., Mol Ther Methods Clin Dev., 2025)
劲帆生物医药科技(武汉)有限公司简称“劲帆医药”,创立于2022年,提供一站式病毒载体、蛋白和疫苗CRO/CDMO服务,拥有全球领先的规模化AAV制备专利技术平台及病毒载体/cGMP级蛋白/疫苗生产车间,致力于推进基因治疗药物、蛋白药物、治疗性疫苗更有效,更安全,更经济,更可及,赋能客户,造福患者。劲帆医药cGMP生产车间,包括4个P2级别种子建库区、5条蛋白/病毒生产线和1条灌装生产线,蛋白/病毒生产线生产规模分别为200 L和500 L,年最大产能可达50批次,目前已完成多项项目交付。
十多年前的初步非人灵长类动物研究表明,即使动物体内预先存在低水平的抗AAV9 NAbs,也可以通过鞘内注射的方式注射AAV9载体,而不会出现任何可测量到的转导抑制。这与静脉注射AAV的普遍认知相悖:人们普遍认为存在一个明确的抗AAV抗体阈值,超过该阈值会显著抑制AAV载体的生物分布,因此预先存在抗体的患者应被排除在临床试验之外。使用其他给药途径的临床试验通常也会因出于谨慎考虑,或只是为了遵循其他既定的先例,而采用与静脉注射临床试验类似的标准排除血清阳性受试者。然而,其他一些试验以及美国食品药品监督管理局(FDA)批准的基因治疗药物并未排除血清阳性患者。例如用于治疗莱伯氏先天性黑蒙的视网膜下注射型AAV2载体药物Luxturna,其FDA批准的禁忌症中并未将AAV2血清阳性列为禁忌症。同样,用于治疗芳香族L-氨基酸脱羧酶(AADC)缺乏症的壳核内注射型AAV2载体药物Kebilidi,其FDA批准的禁忌症中也未将AAV2血清阳性列为禁忌症。然而,Kebilidi的药品说明书指出,“目前尚无足够数据确定抗AAV2抗体对药物的药代动力学、药效学、安全性或有效性的影响。”目前,临床试验的结果差异很大,有些试验排除了血清阳性受试者,而有些试验则纳入了这些受试者。首例鞘内基因治疗试验针对巨轴突神经病(GAN)测试了鞘内注射AAV9/GAN载体的疗效,而该试验并未排除血清阳性受试者。虽然试验参与者总数有限(n = 14),但43%的入组受试者在基线时血清呈阳性,且治疗的安全性和有效性与基线抗AAV9血清阳性率之间无明显相关性。在一名基线血清阳性的受试者中,尸检分析显示中枢神经系统载体DNA的生物分布与临床前研究结果一致,但除脾脏外,大多数外周器官的生物分布极低(每个细胞<0.01 vg拷贝)。这些非常有限的临床经验表明,鞘内注射AAV(至少是AAV9)可以安全有效地靶向中枢神经系统。
Vono等人旨在通过对三组食蟹猴进行scAAV9-CBA-mCherry载体生物分布研究,探讨预先存在的血清AAV9抗体的影响。三组分别为低血清阳性组(总抗AAV9抗体[TAb]≤1:20)、中血清阳性组(TAb 1:160–1:640)和高血清阳性组(TAb 1:40960–1:327680)。每只食蟹猴接受1.2×10¹³ vg的剂量,且未接受任何免疫抑制治疗。试验结果显示,低血清阳性组和中血清阳性组动物的脑脊液(CSF)中未检测到TAb,而高血清阳性组动物的CSF TAb滴度范围为1:160至1:640。就载体生物分布而言,各组间脑和脊髓的载体分布均无统计学意义上的显著差异;在外周器官和背根神经节中,中等血清阳性组的载体生物分布始终呈下降趋势,而高血清阳性组的载体生物分布则显著低于其他组。值得注意的是脾脏,其载体生物分布随预先存在的TAbs水平升高而增加,这与GAN临床试验中n=1的观察结果相似。总体而言,包括临床评估、血液化学和组织病理学在内的安全性评估未发现与较高水平的预先存在的TAbs相关的任何重大安全性问题。值得注意的是,高血清阳性组动物的脑膜和/或神经毡血管周围区域的单核细胞浸润程度有增加的趋势,但这些变化无症状,且被判定为非不良反应。
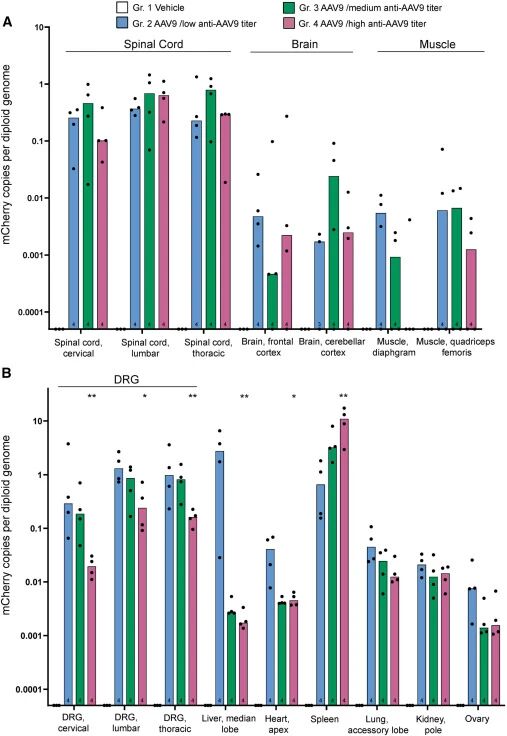
图1 四周时Vg生物分布
(图片来源:Maria Vono et al., Mol Ther Methods Clin Dev., 2025)
在免疫反应方面,高血清阳性组与低血清阳性组和中血清阳性组存在一些差异:高血清阳性组的抗AAV9 TAb反应更快、强度更高;同样,高血清阳性组中各种CD4+ T细胞亚群的水平也显著升高(图2),并且高血清阳性组的CD8+ T细胞水平也呈现升高的趋势(图3);除高血清阳性组中IP-10、I-TAC、MCP-1和IL-RA的短暂升高外,各组间细胞因子活化水平无差异。各组间补体活化水平也无差异(图4)。
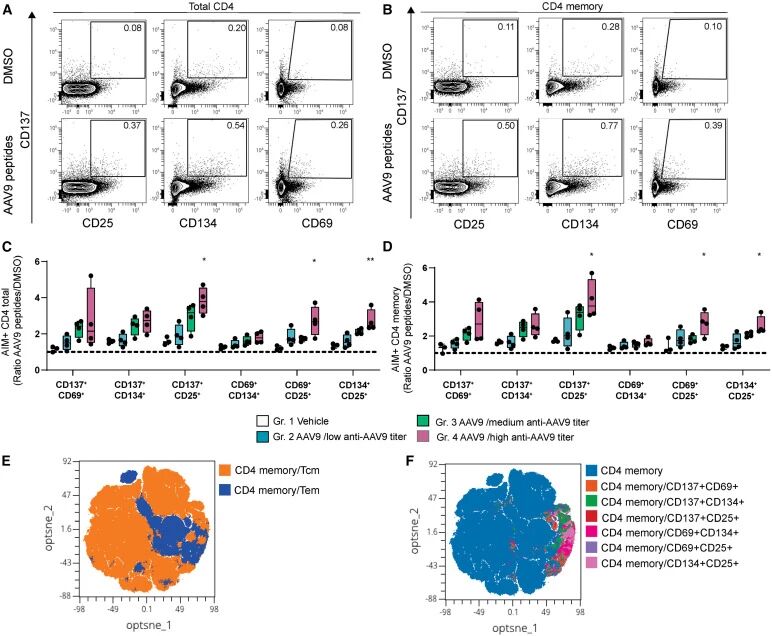
图2 在预先存在高水平抗AAV9抗体的免疫动物的脾脏中观察到更强的AAV9特异性CD4 T细胞反应
(图片来源:Maria Vono et al., Mol Ther Methods Clin Dev., 2025)
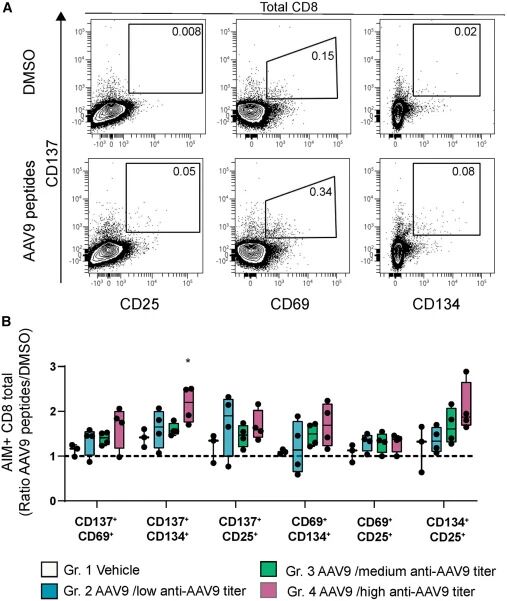
图3 脾脏中AAV9特异性CD8 T细胞反应
(图片来源:Maria Vono et al., Mol Ther Methods Clin Dev., 2025)
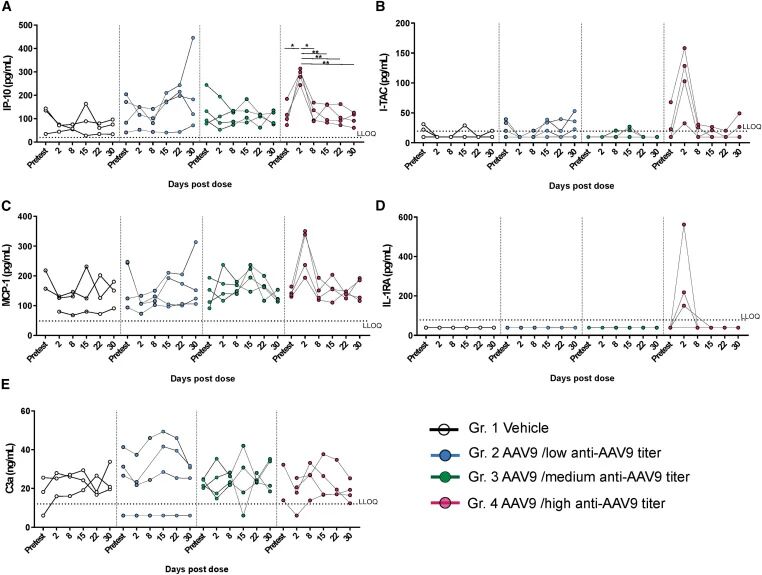
图4 血浆细胞因子和补体因子C3a的纵向评估
(图片来源:Maria Vono et al., Mol Ther Methods Clin Dev., 2025)
如果预先存在的AAV血清阳性率被列为排除标准和/或禁忌症,许多患者可能将被排除在经内递送基因治疗之外。例如,AAV9 NAb在普通人群中的血清阳性率约为35%。随着经鞘内递送AAV的临床试验数量的增加,患者排除的影响也日益显著,这个问题亟需明确的答案。Vono等人迄今为止对此进行了最全面的临床前评估,其总体结论是,这些血清阳性患者可以安全地接受这些治疗,并有望获得中枢神经系统靶向获益。但仍存在一些注意事项和关键的未解之谜。考虑到血清阳性个体中载体向外周器官的生物分布受到限制,如果外周器官(或外周神经系统)转导介导了部分整体治疗效果,那么这些个体的整体获益可能会降低。另一个问题是,非人灵长类动物研究的变异性通常很高,而Vono等人发表的研究也存在类似的问题。本研究也不例外。研究结论认为,血清阳性动物的中枢神经系统转导未受到显著抑制(即无统计学意义上的差异),但该研究样本量不足以探讨是否存在更为轻微(例如,2倍)的中枢神经系统生物分布降低。下一个合乎逻辑的问题是,受试者是否可以通过鞘内给药途径再次给药。Vono等人发现,在TAb血清滴度>1:40960的动物中,AAV9仍能显著分布于中枢神经系统,这可能合理地代表了鞘内给药AAV9后TAb的水平。因此,本研究对再次给药问题的初步回答是肯定的。但需要特别注意的是,重复给药可能会出现轻微但有意义的中枢神经系统生物分布降低,而本研究样本量不足以检测到这种降低,因此应在未来的临床前研究中直接验证再次给药方案。总体而言,即使存在这些注意事项和未解答的问题,这项研究的结果仍然利好于有望采用鞘内注射的AAV基因治疗获益的患者。
原文链接:
https://www.cell.com/molecular-therapy-family/advances/fulltext/S2329-0501(25)00226-8
https://www.cell.com/molecular-therapy-family/advances/fulltext/S2329-0501(25)00197-4

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。