2026-04-13
在基因治疗的临床转化进程中,确定安全且有效的中枢神经系统(CNS)给药剂量一直是业界公认的核心挑战。近期,渤健(Biogen)研究团队在《Molecular Therapy》期刊上发表了题为《Identification Of a Therapeutic Threshold For AAV-STXBP1 Gene Therapy in a Rodent Model of STXBP1 Developmental & Epileptic Encephalopathy》的突破性研究。该研究利用AAV基因补充疗法在STXBP1发育性癫痫性脑病(STXBP1-DEE)小鼠模型中实现了长效的表型逆转,并首次定量界定了实现疾病挽救所需的“皮层神经元转导阈值”。这一发现为AAV基因治疗的临床前药效评价及大动物剂量折算提供了极其关键的定量标尺。
研发背景:基因补充疗法的临床转化痛点
STXBP1-DEE是一种高发的遗传性癫痫及神经发育障碍疾病,其发病机制主要源于STXBP1基因的杂合功能丧失突变。STXBP1蛋白在CNS中广泛表达,通过与SNARE蛋白突触体相关蛋白1(Syntaxin-1, STX1)直接结合,调节突触小泡的外排和神经递质的释放。目前,该疾病尚无获批的疾病修饰疗法。
利用AAV病毒载体直接提高CNS中STXBP1的表达是极具潜力的治疗策略。然而,AAV载体的剂量相关毒性始终是悬在研发者头顶的达摩克利斯之剑。此前,一项旨在增强STXBP1表达的靶向大脑AAV基因治疗临床试验,因发生患者死亡的严重不良事件而被迫终止。这一挫折凸显了明确AAV介导的STXBP1表达“治疗阈值”的迫切性:究竟需要转导多大比例的神经元,才能在确保安全的前提下实现有临床意义的表型逆转?
核心数据解析
该研究选用Stxbp1+/-小鼠作为疾病模型。该模型能够高度再现人类患者的关键病理表型,包括皮层过度兴奋(脑电图表现为棘慢波放电,SWDs)、运动功能障碍和认知受损。
1. 概念验证:hSyn启动子介导的精准表达与表型逆转(图1-3)
研究首先构建了携带人类STXBP1亚型B编码序列的AAV-PHP.B载体,由人突触素1(hSyn)神经元特异性启动子驱动,通过出生后第0/1天(PND0/1)的脑室内(ICV)注射给药。
组织级表达:AAV-PHP.B-hSyn-STXBP1治疗在小鼠皮层中引起了DNA载体分布、转基因mRNA水平的剂量依赖性增加(图1B, 1C)。总STXBP1蛋白及药效学标志物STX1蛋白也呈现剂量依赖性上升(图1D, 1E)。
细胞嗜性与转录组逆转:单核转录组学(snRNAseq)表明,在3×1010vg/mouse剂量下,平均49.0%的皮层谷氨酸能神经元和32.4%的GABA能神经元被成功转导,而胶质细胞中的转导率接近于零(图2A)。这种神经元特异性转导有效逆转了疾病模型皮层中异常的分子特征。
表型全面获益:Stxbp1+/-小鼠表现出极高的异常棘慢波放电(SWDs)。经治疗后,所有剂量组均将SWD显著降低至野生型水平(图3B)。此外,治疗显著改善了小鼠的运动潜伏期(图3C),并在较高剂量下显著改善了认知学习缺陷(图3D, 3E)。
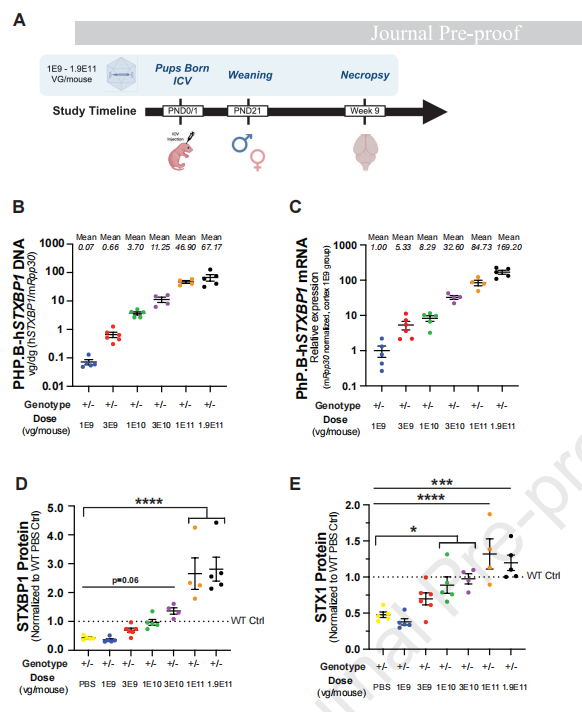
图1 对Stxbp1杂合缺陷小鼠进行新生鼠颅内侧脑室注射AAV-PHP.B-hSyn-STXBP1,可剂量依赖性上调小鼠大脑内STXBP1与STX1蛋白表达
(图片来源:Gallo NB et al, Mol Ther., 2026)
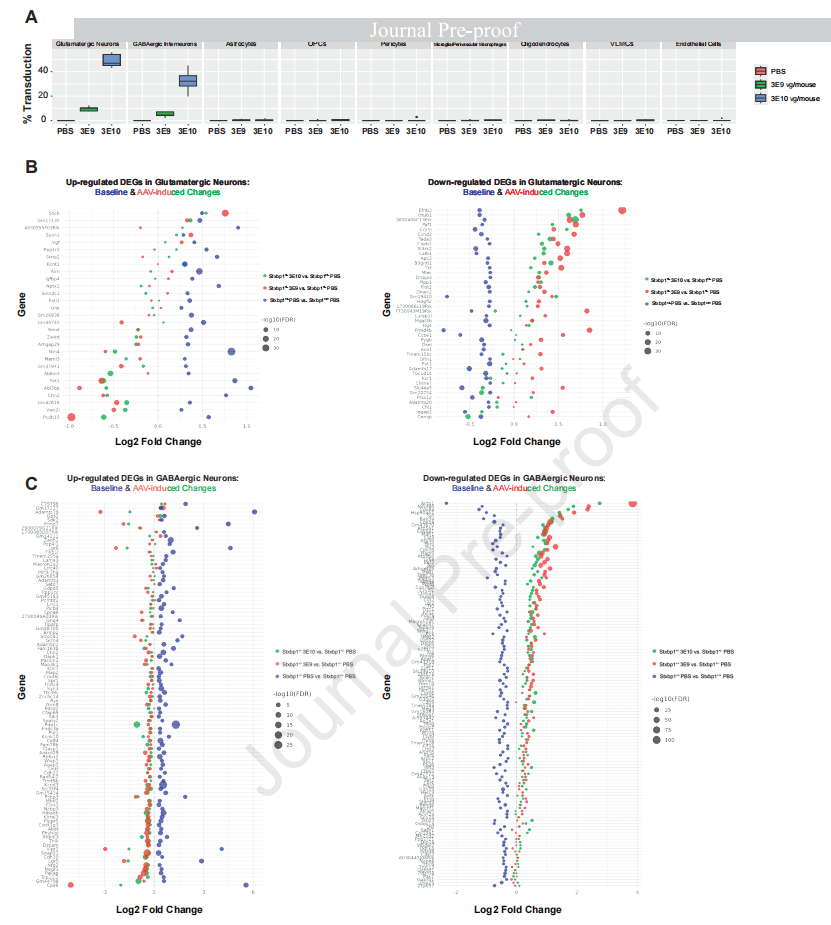
图2 人突触核蛋白1启动子可介导腺相关病毒转基因在兴奋性神经元和抑制性神经元中表达,部分逆转Stxbp1杂合缺陷小鼠的转录组改变
(图片来源:Gallo NB et al, Mol Ther., 2026)
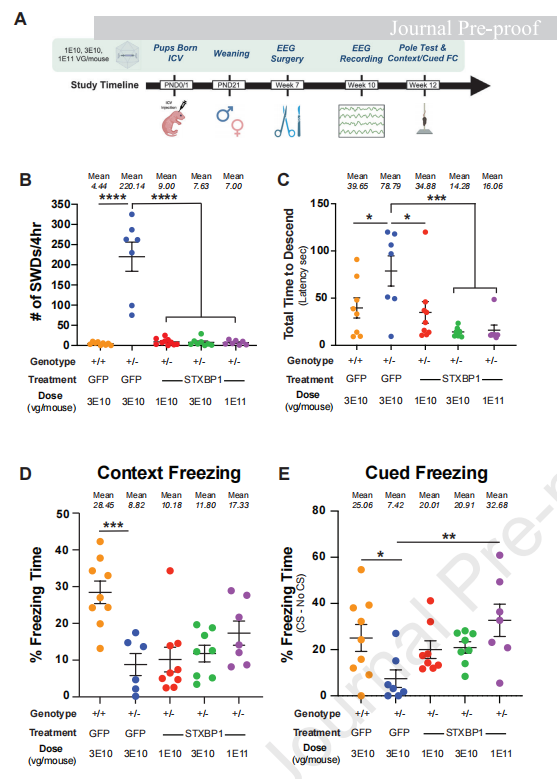
图3 AAV-PHP.B-hSyn-STXBP1 可挽救Stxbp1杂合缺陷小鼠的脑电图异常及行为学表型
(图片来源:Gallo NB et al, Mol Ther., 2026)
2. 关键突破:确立“44%转导率”的定量治疗阈值(图4)
为提高临床转化价值,研究换用临床验证的AAV9衣壳,搭载相同基因表达盒进行精细剂量范围研究。
药效学剂量响应:AAV9同样剂量依赖性地减少了SWD发生率。在2×109、5×109和1×1010vg/mouse剂量下,SWD分别下降了13.2%、59.4%和62.2%,统计学显著性在5×109vg/mouse 剂量组开始显现(图4B)。运动功能评估也呈现出平行的剂量依赖性改善(图4C)。
高分辨率皮层神经元转导定量:研究采用多重RNAscope荧光原位杂交(针对AAV 3' UTR中的WPRE元件)联合NeuN抗体免疫荧光染色(图4H)。通过U-Net神经网络算法识别NeuN阳性细胞并计算WPRE共表达率,实现了自动化定量。
明确的治疗阈值:结果显示,随着AAV9剂量递增,皮层神经元转导率依次为22.87%(2×109)、44.26%(5×109)和63.13%(1×1010)(图4I)。表型改善与转导率呈强相关(图4J, 4K)。这一数据确立了明确的量化阈值:需至少44%的皮层神经元转导率,才能显著改善过度兴奋及运动表型。
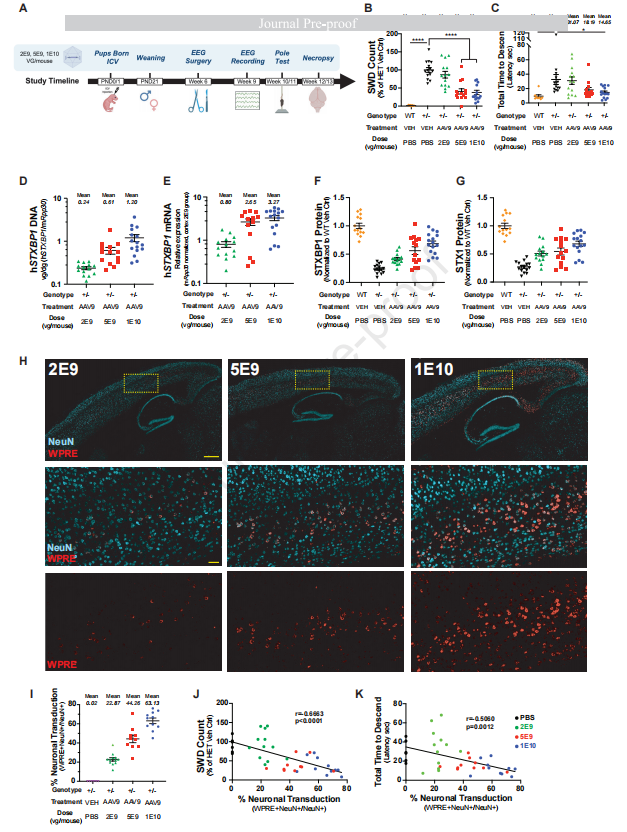
图4 通过AAV9-hSyn-STXBP1剂量梯度试验,明确了挽救Stxbp1杂合缺陷小鼠癫痫与运动表型所需的皮层神经元转导最低阈值
(图片来源:Gallo NB et al, Mol Ther., 2026)
3. 体内表达的长期持久性(图5)
对AAV9治疗后1个月、6个月和12个月的表达动力学追踪显示:
基因组与表达产物的动力学:皮层中的病毒DNA水平在第1个月至第6个月期间显著下降并随后稳定(图5B),反映了未能形成稳定游离体(episomes)的基因组被自然清除。相反,转基因mRNA、STXBP1蛋白和STX1蛋白在第1至6个月期间呈上升趋势,并在此后长达一年内保持稳定(图5C-E)。
神经元转导率长效稳定:在长达一年的观察期内,皮层中表达STXBP1转基因的神经元比例保持稳定,未出现显著的时间依赖性丢失(图5F, 5G)。长期表达未引发显著的神经炎症,支持了该策略的长期安全性。
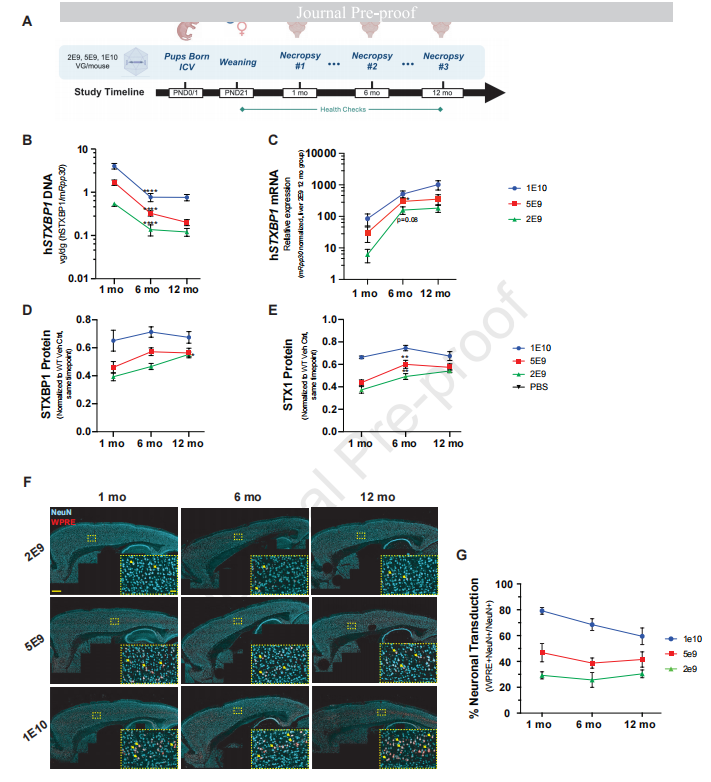
图5 新生鼠颅内侧脑室注射AAV9-hSyn-STXBP1后,可在Stxbp1杂合缺陷小鼠大脑皮层中实现长效转基因表达
(图片来源:Gallo NB et al, Mol Ther., 2026)
在中枢神经系统基因治疗试验中,直接获取脑组织以评估靶点结合是不现实的,CSF标志物的开发至关重要。
鼠源CSF的靶点验证:利用定制的MSD分析法显示,给予AAV9后,不仅小鼠皮层中的STXBP1水平升高,其CSF中的STXBP1蛋白浓度也实现了显著增加(图6A, 6B)。
人源CSF的质谱(LC/MS)验证:研究建立了一种定量的液相色谱-平行反应监测质谱法,成功在健康人类供体的CSF样本中同时检测并定量了STXBP1及其核心互作蛋白STX1A和STX1B(图7)。这意味着未来临床试验有望通过检测CSF无创评估药物的靶点表达与下游生理功能的恢复。
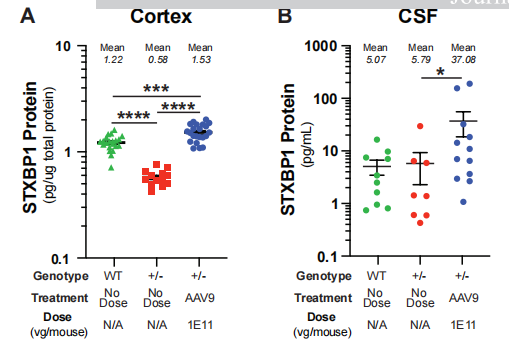
图6 AAV9-hSyn-STXBP1可提升Stxbp1杂合缺陷小鼠脑脊液中STXBP1蛋白水平
(图片来源:Gallo NB et al, Mol Ther., 2026)
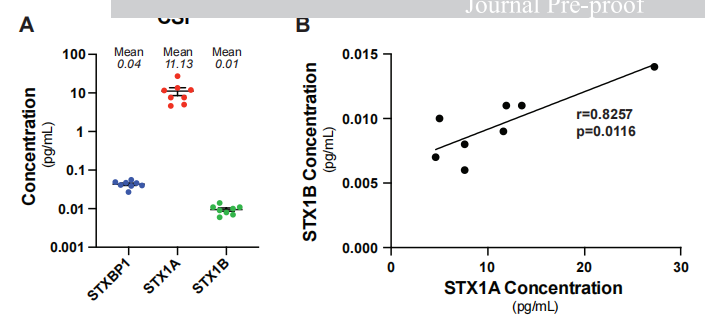
图7 可通过质谱技术在人体脑脊液中检测到STXBP1与STX1蛋白
(图片来源:Gallo NB et al, Mol Ther., 2026)
启示与结语
本项严谨的临床前研究对整个神经系统AAV基因治疗的研发路径提供了极具参考价值的范式。由于缺乏精确的空间定量工具,行业内很难将啮齿类动物的有效剂量平移至大型动物或人类。该研究结合RNAscope原位杂交与人工智能图像分析,将抽象的有效性具象化为“44%的皮层神经元转导率”这一硬性指标。该技术框架具有极强的通用性,通过检测通用的WPRE序列,这套评估体系可以轻松适配至其他致病基因或新衣壳的药效评估中。
伴随长期稳定表达的耐久性数据以及具有极高转化价值的CSF生物标志物检测方法的建立,这项工作为攻克STXBP1-DEE及其他重度神经发育障碍疾病奠定了坚实的科学基础。基因治疗在CNS领域的深入拓展,正在迎来更加精细化和定量化的新纪元。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。