2026-04-22
近日,Communications Biology(2025)发表了题为《OPTN protects retinal ganglion cells and ameliorates neuroinflammation in optic neuropathies》的研究。该研究首次明确野生型视神经蛋白(OPTN)在维持视网膜神经节细胞(RGC)存活与视网膜神经免疫稳态中的核心作用,揭示了OPTN介导的非眼压依赖型神经保护机制,为青光眼等视神经病变的治疗提供了新靶点。

(图片来源:Wang Q et al, Commun Biol., 2025)
一、研究背景与核心问题
OPTN作为一种关键接头蛋白,参与NF-κB信号通路、自噬等多种细胞过程,其突变与原发性开角型青光眼(POAG)、肌萎缩性脊髓侧索硬化症(ALS)等疾病密切相关。目前已知ALS中OPTN突变以“功能缺失”为主,而POAG中仅报道“功能获得”机制。
视网膜神经节细胞(RGC)的退行性变是青光眼等视神经病变的核心病理特征,最终导致不可逆视力丧失。尽管已有体外研究提示野生型OPTN可能具有神经保护作用,但其一,体内对RGC稳态的调控作用缺乏直接证据;其二,OPTN是否通过“功能缺失”机制参与POAG发病尚不明确;其三,OPTN在视网膜神经免疫稳态中的作用仍属未知。基于此,本研究聚焦野生型OPTN对RGC存活及神经炎症的调控作用,探究其在正常眼压性青光眼(NTG)与高眼压性青光眼(HTG)中的共同作用机制。
二、核心研究结果
本研究通过OPTN条件性敲除小鼠、高眼压模型及分子生物学技术,结合生物信息学分析,得出以下关键结论:
1. OPTN功能缺失导致慢性RGC丢失,且不影响眼压
对1月龄OPTN条件性敲除小鼠进行玻璃体腔注射AAV2-Cre(获得C端截短型OPTN),对照组注射AAV2-PLAP(图1a)。结果显示,注射1个月后OPTN阳性RGC比例显著下降,且RGC数量随时间进行性减少,而对照组无明显变化(图1b、1c);全程监测眼压发现,OPTN敲除未引起眼压改变(图1d),与NTG的病理特征一致,提示OPTN功能缺失介导非眼压依赖型RGC损伤。
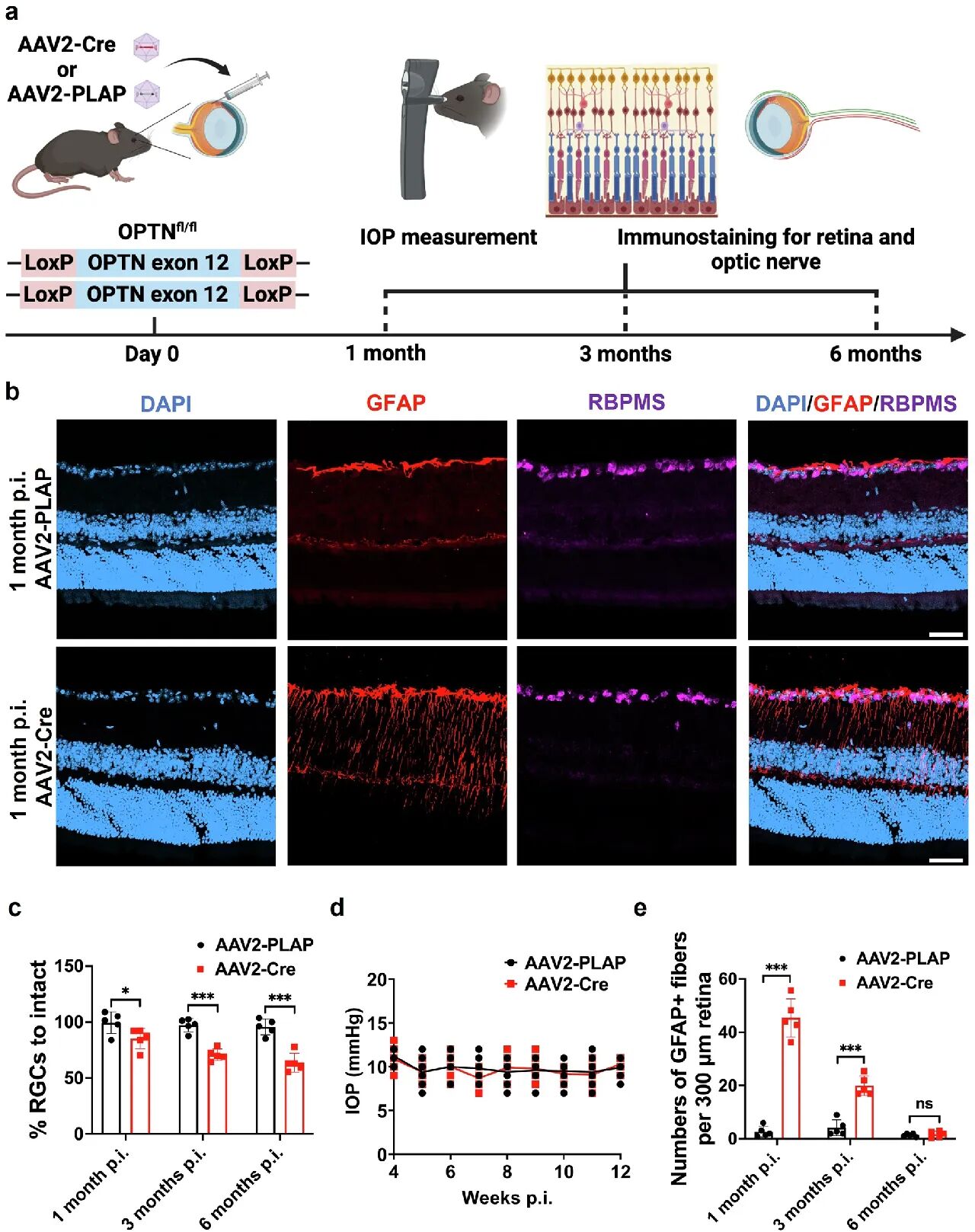
图1 OPTN功能丧失导致RGC丢失和星形胶质增生
(图片来源:Wang Q et al, Commun Biol., 2025)
2. OPTN功能异常诱导视网膜胶质细胞异常反应,且存在时效差异
(1)短期星形胶质细胞增生:OPTN敲除后,GFAP标记的星形胶质细胞出现显著反应性增生,1个月达到峰值,6个月恢复至对照组水平(图1e),提示该反应具有可逆性(图1b)。
(2)长期小胶质细胞激活:OPTN敲除后,CD68标记的激活型小胶质细胞比例显著升高,且持续至6个月(图2a、2c);小胶质细胞呈现胞体增大、突起缩短的阿米巴样激活形态,但数量无显著变化(图2d-f),证实OPTN缺失会引发持续性神经炎症(图2b)。
(3)视神经炎症扩散:OPTN敲除3个月后,视神经中出现小胶质细胞激活,但未引发星形胶质细胞增生(图3a-d),提示视网膜OPTN可调控小胶质细胞激活通路,且炎症反应可扩散至视神经。
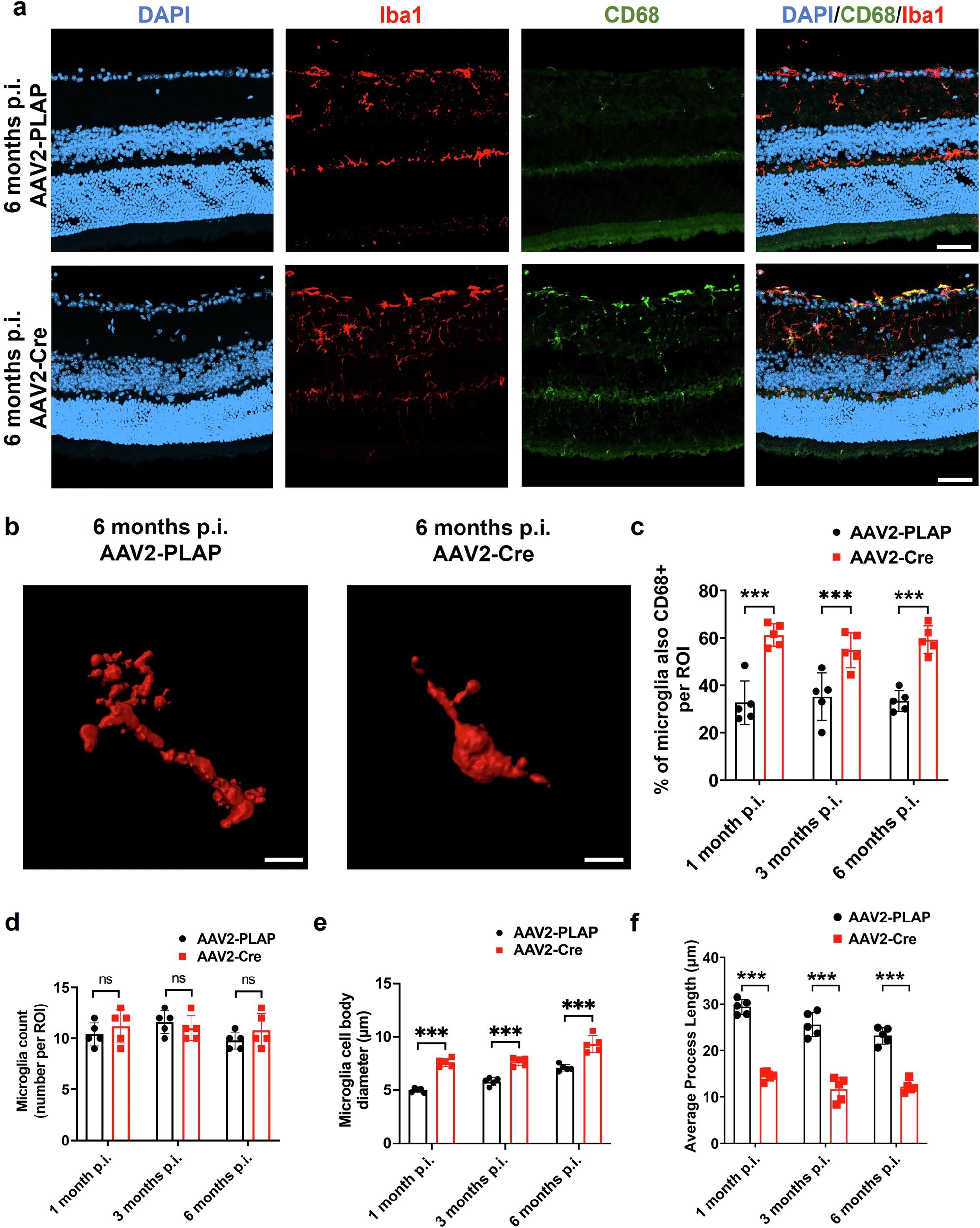
图2 OPTN功能丧失导致小胶质细胞活化
(图片来源:Wang Q et al, Commun Biol., 2025)
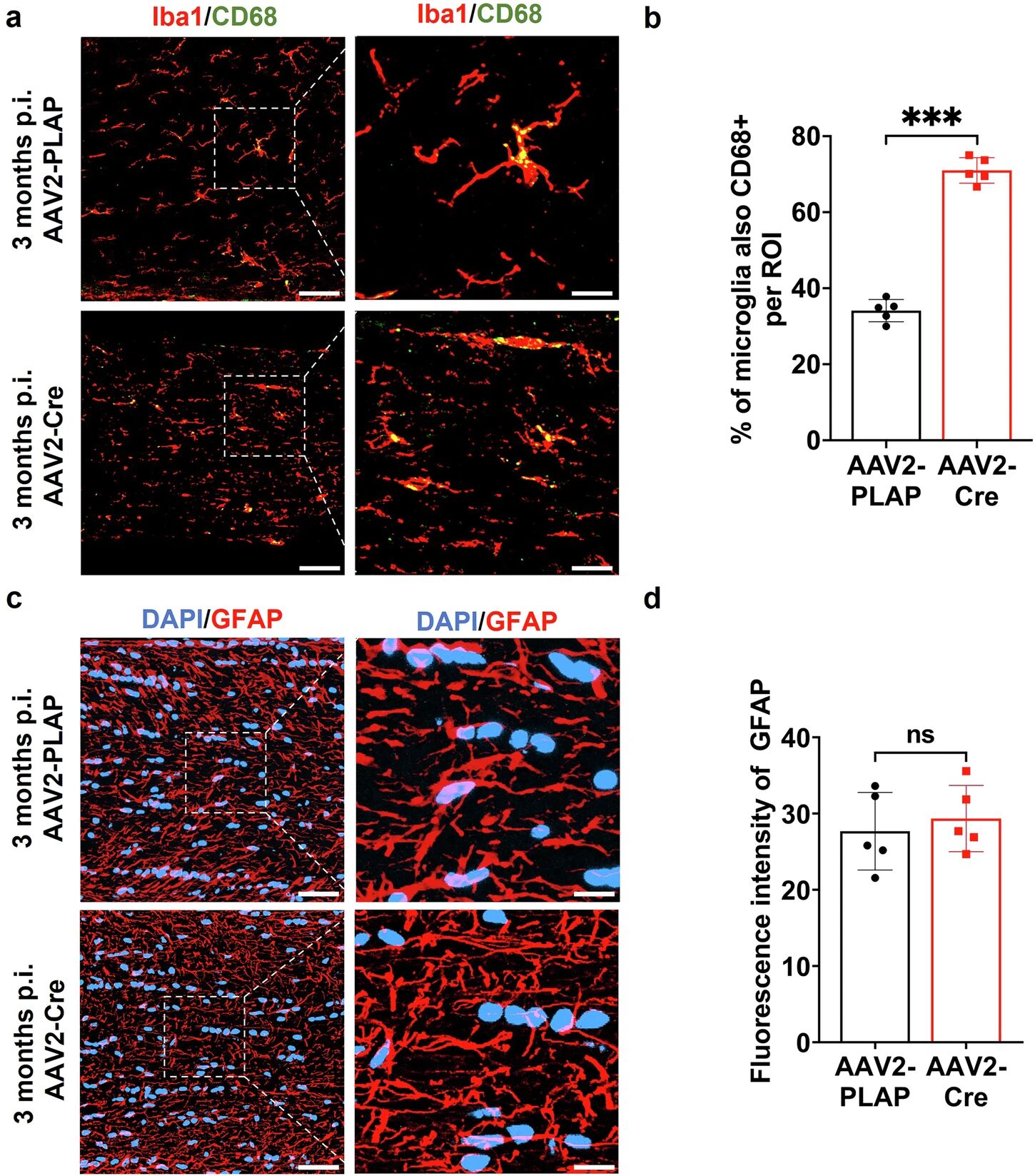
图3 OPTN功能丧失导致视神经中小胶质细胞活化
(图片来源:Wang Q et al, Commun Biol., 2025)
3. OPTN功能缺失不加剧高眼压诱导的RGC死亡
采用优化的黏弹性微珠注射模型构建HTG(图4a、4c),在OPTN敲除1个月后注射微珠,结果显示:微珠注射后眼压显著升高(图4d),但OPTN敲除组与野生型组的RGC存活率无显著差异(图4b、4e),提示高眼压与OPTN功能缺失可能影响同一群脆弱RGC,二者存在共同的基因调控通路。
进一步分析发现,OPTN功能异常与高眼压诱导的星形胶质细胞增生(图5a、5b)、小胶质细胞激活(图6a、6b)模式相似,提示OPTN介导的神经炎症通路是NTG与HTG共有的发病机制。
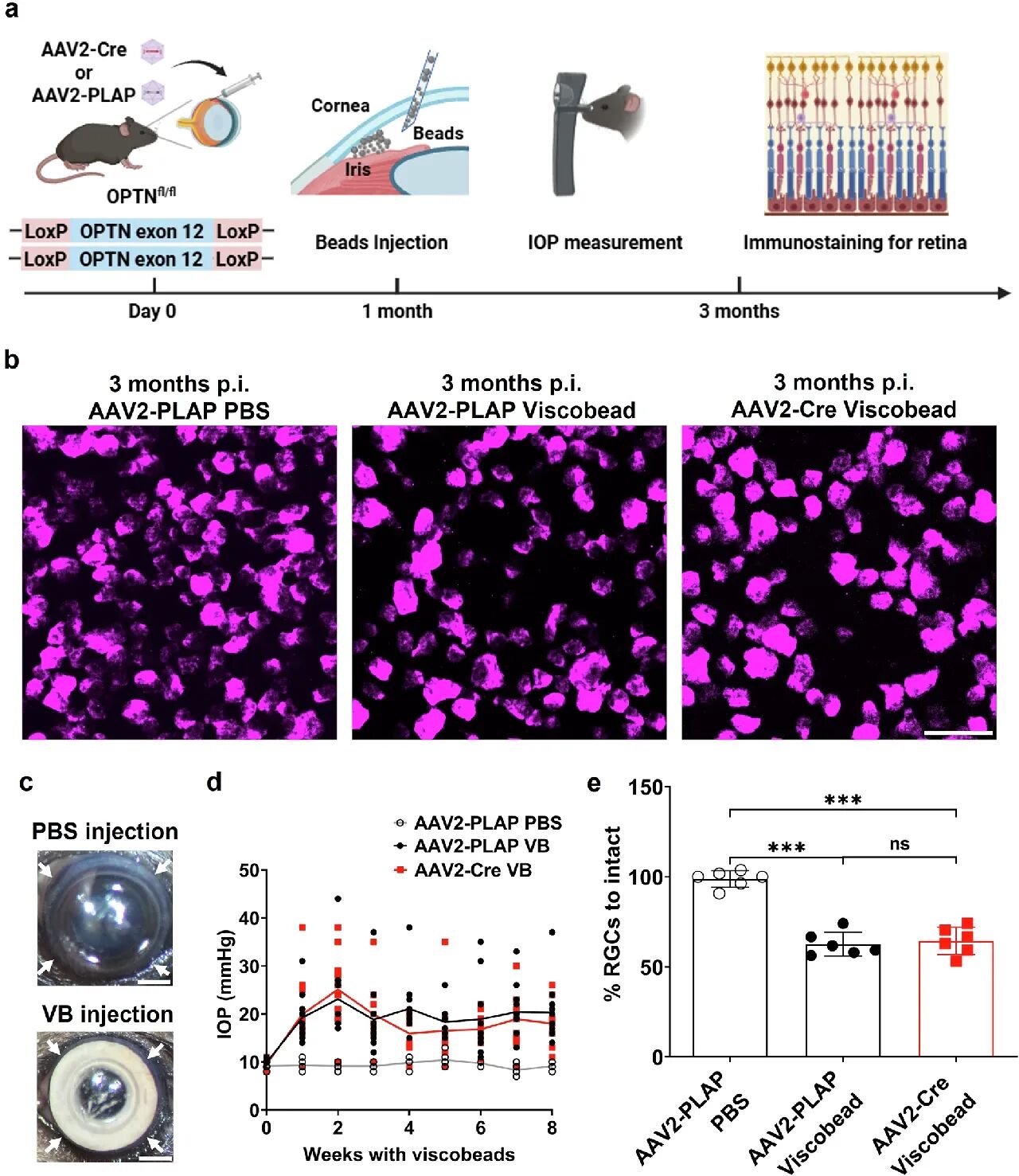
图4 在眼高压小鼠模型中,OPTN功能障碍不会进一步加剧RGC死亡
(图片来源:Wang Q et al, Commun Biol., 2025)
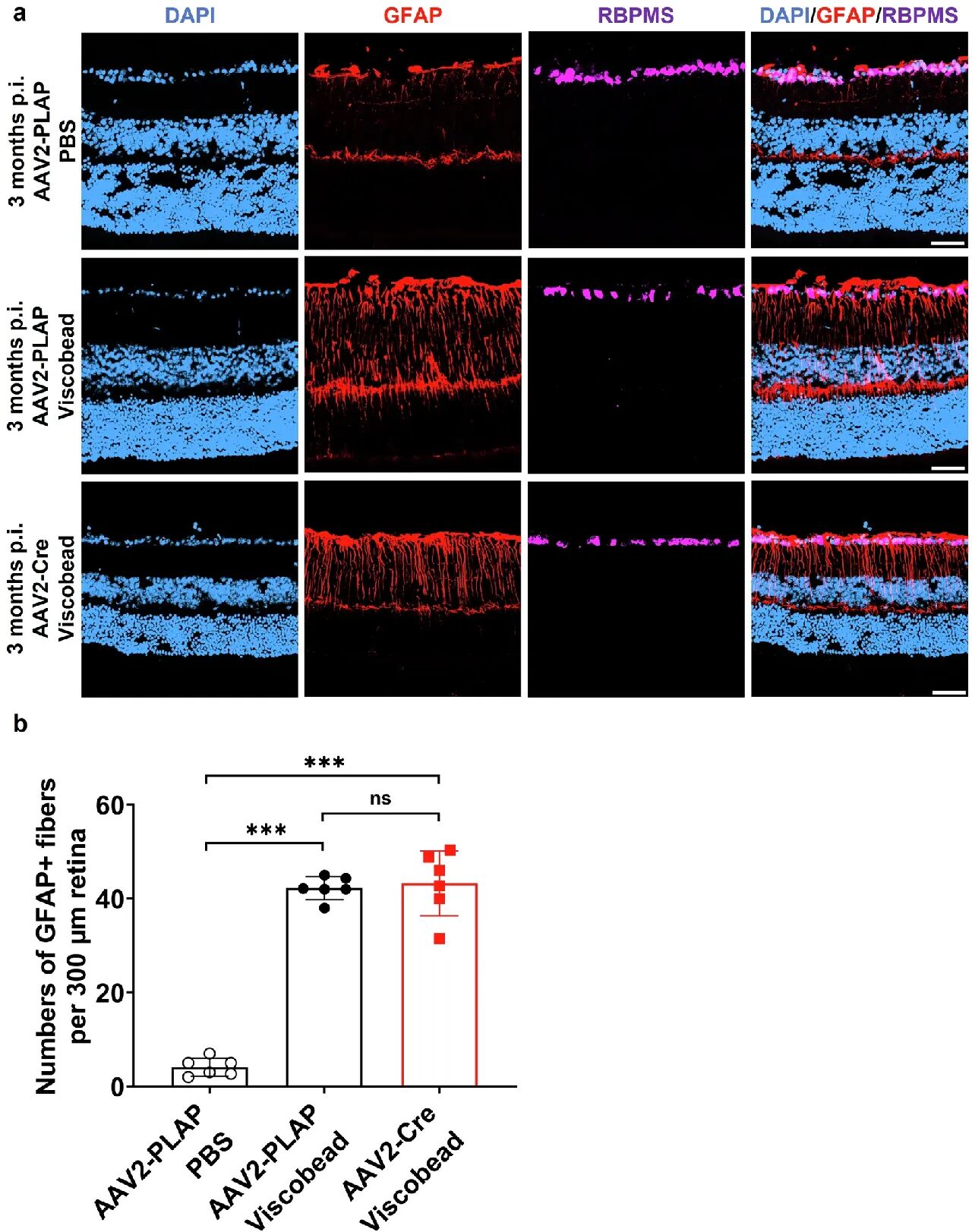
图5 OPTN功能障碍和眼压升高在视网膜中诱发了类似的星形胶质增生模式
(图片来源:Wang Q et al, Commun Biol., 2025)
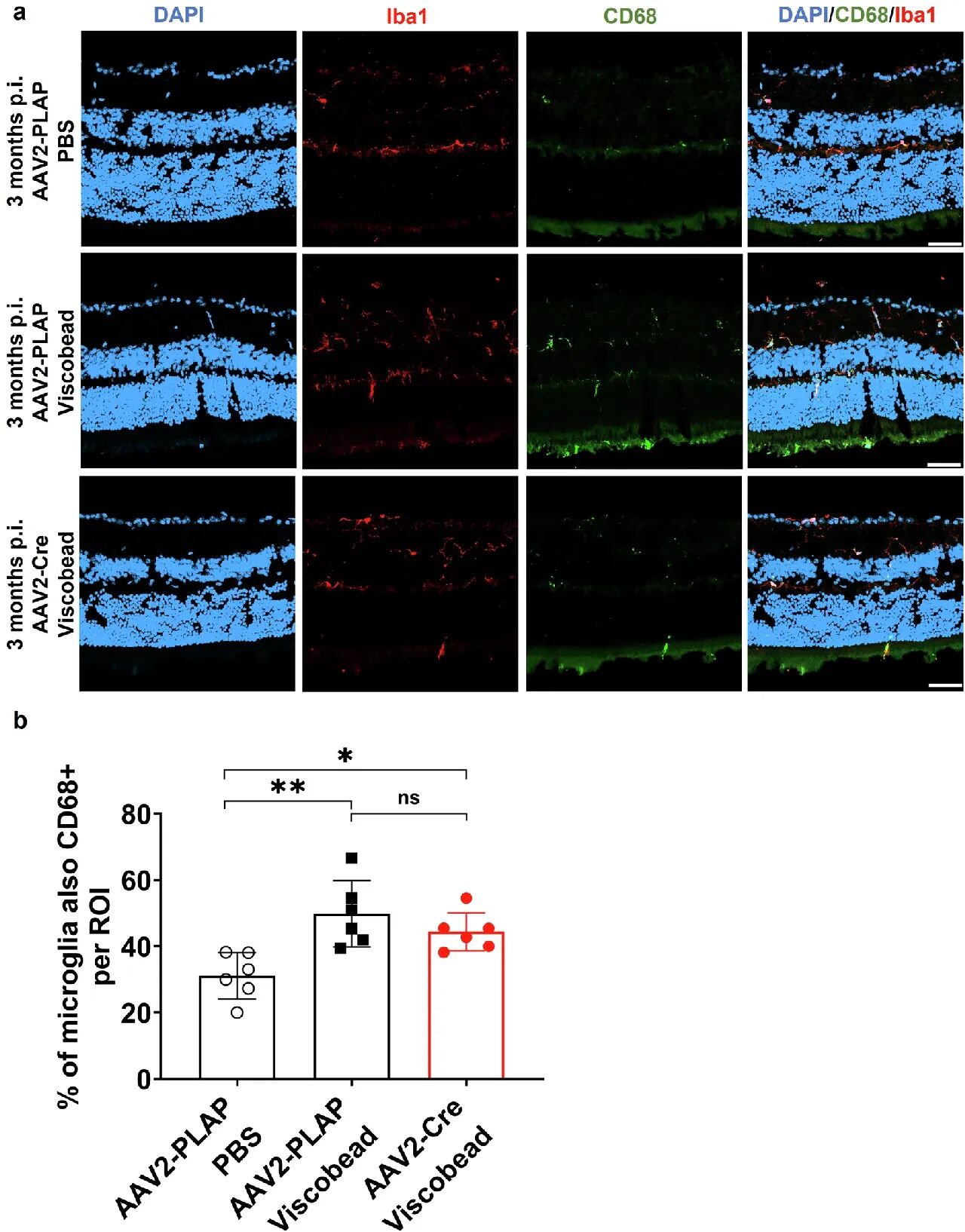
图6 OPTN功能障碍和眼压升高在视网膜中诱发了类似的微胶质细胞活化模式
(图片来源:Wang Q et al, Commun Biol., 2025)
4. OPTN通过调控NPY-CHOP通路维持视网膜神经免疫稳态
单细胞RNA测序(scRNA-seq)分析显示,OPTN在视神经夹伤(ONC)模型的耐受型RGC中富集,且损伤后表达升高(图7a);差异表达基因分析发现,神经肽Y(NPY)与趋化因子FAM19A4在OPTN阳性RGC中显著高表达(图7b、7c)。
临床数据集验证显示,NTG患者RGC中OPTN、NPY与FAM19A4均显著下调(图7d);动物实验证实,OPTN敲除3个月后,视网膜神经节细胞层(GCL)与内丛状层(IPL)中NPY表达显著下降(图7e、7f)。同时,OPTN功能缺失会激活CHOP信号通路,但不影响ATF3表达,提示OPTN-NPY通路可能通过抑制CHOP介导的神经炎症,维持视网膜稳态。
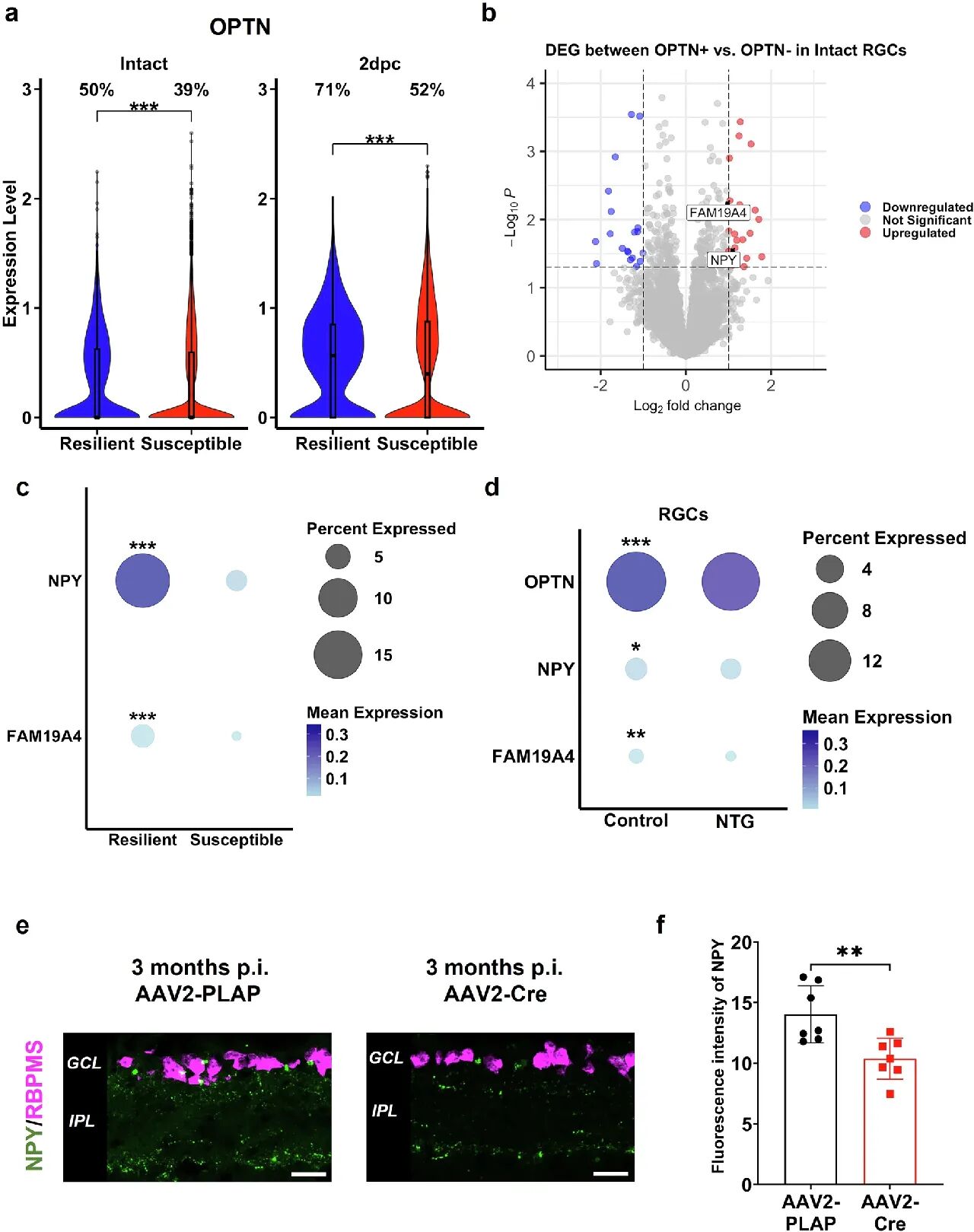
图7 对RGC和IF的scRNA-seq数据集进行生物信息学分析,验证OPTN敲除后NPY的表达水平
(图片来源:Wang Q et al, Commun Biol., 2025)
5. 过表达野生型OPTN可挽救高眼压诱导的RGC损伤
采用CPP16衣壳修饰型AAV载体,在小鼠视网膜过表达人源野生型OPTN(图8a),结果显示:野生型OPTN过表达可显著缓解高眼压诱导的RGC丢失与小胶质细胞激活,但不影响星形胶质细胞增生(图8b-d);且各组眼压无显著差异,证实其保护作用不依赖眼压调节。此外,过表达NTG相关E50K OPTN突变体未加剧病理损伤,提示其与高眼压型青光眼存在重叠病理机制。
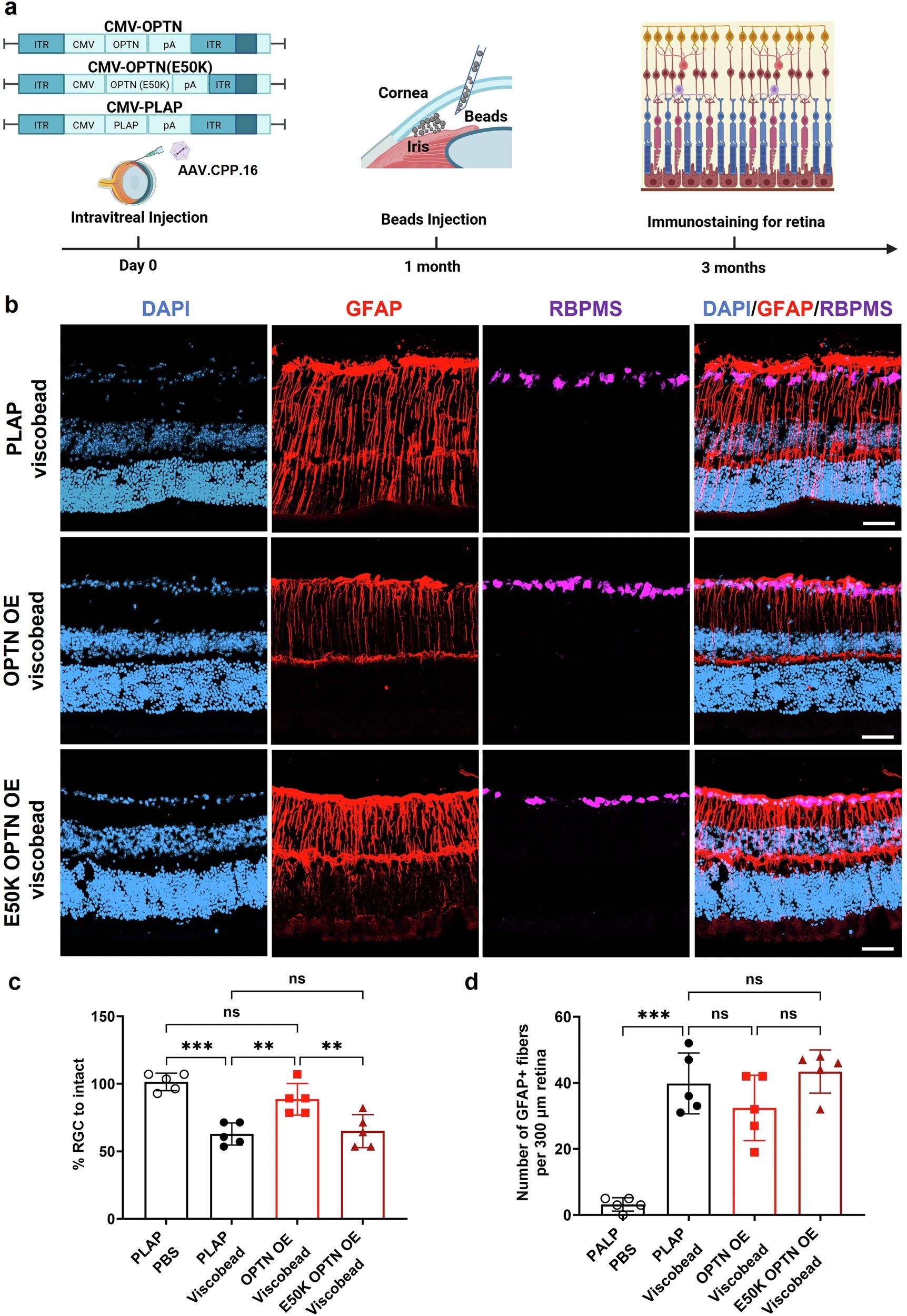
图8 野生型OPTN的过表达挽救了粘珠注射引起的眼高压模型中的RGC丢失,但未能挽救星形胶质细胞增生
(图片来源:Wang Q et al, Commun Biol., 2025)
三、研究结论与意义
本研究核心结论:野生型OPTN是维持RGC存活与视网膜神经免疫稳态的关键神经免疫调控因子,其功能缺失可通过下调NPY、激活CHOP通路,引发持续性神经炎症与RGC退行性变;而过表达野生型OPTN可通过抑制小胶质细胞激活,发挥非眼压依赖的神经保护作用。
研究意义在于:
① 补充了OPTN突变的“功能缺失”机制在POAG中的作用,证实OPTN可通过两种机制参与视神经病变;
② 揭示了OPTN-NPY-CHOP通路作为NTG、HTG共有的发病机制,为青光眼(尤其是降眼压治疗无效病例)提供了新的治疗靶点;
③ CPP16衣壳AAV介导的OPTN过表达具有良好的跨物种转化潜力,为基因治疗提供了新策略。
四、研究方法概要
本研究采用OPTN条件性敲除小鼠,通过玻璃体腔AAV注射实现OPTN敲除或过表达,利用黏弹性微珠注射构建HTG模型;结合免疫荧光染色、scRNA-seq、生物信息学分析等技术,检测RGC存活、胶质细胞激活及相关分子表达;统计分析采用t检验、单因素/双因素ANOVA等方法,确保实验可重复性。
参考文献
Wang Q, Wang Y, Jiang YDD, Donahue R, Cao G, Yan W, Guo H, Li Z, Liang J, Hao J, Lu Y, Bei F, Wang Q, Tian F. OPTN protects retinal ganglion cells and ameliorates neuroinflammation in optic neuropathies. Commun Biol. 2025 Oct 16;8(1):1475. doi: 10.1038/s42003-025-08534-6. PMID: 41102382; PMCID: PMC12533019.

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。